до какого возраста может проявиться сма
Спинальная мышечная атрофия (СМА): ответы на самые часто задаваемые вопросы
Эту болезнь называют самой частой из редких. Она встречается у одного новорождённого из 6 000-10 000. Спинальная мышечная атрофия (СМА) – это наследственное заболевание, связанное с мутациями в гене. У больного постепенно атрофируются мышцы, и он сначала теряет способность ходить, а затем – глотать и дышать. В 2019 году в США изобрели новый препарат от СМА – «Золгенсма». Оно, как утверждают разработчики, не только приостанавливает развитие болезни, но и улучшает общее состояние, практически возвращая больного к обычной полноценной жизни. «Лабиринт 42» подготовил ответы на самые распространённые вопросы об этой коварной болезни.
В чём причина возникновения СМА?
Причина в повреждённом гене SMN1. В результате мутации у человека не вырабатывается белок, который нужен для выживания мотонейронов. Это важная часть спинного мозга человека, от них по длинным нервам идут сигналы к скелетным мышцам организма. В 95 % случаев причиной СМА становится делеция, то есть выпадение участка генетического кода.
Если мотонейрон недополучает достаточного количества белка для своего питания, то он быстро «устаёт». Мотонейроны начинают погибать, они не могут посылать сигналы к скелетным мышцам, благодаря которым человек ходит, сидит, лежит и дышит. Мышцы остаются без работы и постепенно отмирают.
То есть к атрофии мышц приводит дефицит важного белка, который не вырабатывает ген SMN1. Но у человека есть ещё ген SMN2, который дублирует SMN1. Он производит нефункциональный белок и небольшое количество нормального белка, который позволяет мотонейронам человека выживать на очень голодном пайке. В результате человек со СМА может сохранять какую-то часть двигательных, глотательных и дыхательных функций.
Можно ли заранее узнать, будет ли у ребёнка СМА?
Да, ещё в период планирования беременности можно сдать тест на носительство СМА. Дело в том, что если оба партнёра являются носителями этого заболевания, то вероятность рождения у них ребёнка со СМА составляет 25%. В 50% случаев у такой пары родится носитель СМА и в 25% малыш будет совершенно здоровым.
25% – довольно высокий риск, поэтому в этом случае рекомендуют использовать ЭКО – с помощью предимплантационной диагностики на 5-е сутки после оплодотворения яйцеклетки берут материал на анализ ДНК. Для процедуры ЭКО отбирают только эмбрионы без мутаций. Также можно сделать исследование плода на СМА на 11 неделе беременности. Кроме того, недавно Москве запустили пилотную программу тестирования новорождённых на спинальную мышечную атрофию (СМА). Это заболевание пока не включено в обязательный скрининг. В дальнейшем такие исследования могут распространиться на все российские регионы.
От чего зависит степень тяжести болезни?
У человека может быть разное число копий гена SMN2. Чем больше у пациента со СМА таких копий, которые вырабатывают маленькое количество нужного мотонейронам белка, тем легче будет протекать заболевание, тем благоприятнее прогноз.
Существует 4 типа спинальной мышечной атрофии. I тип – самый тяжёлый, проявляется на первых месяцах жизни. IV тип – самый лёгкий, может диагностироваться у взрослых людей.
Как проявляется СМА, каковы его первые симптомы?
Симптоматика зависит от типа заболевания. При первом типе СМА у малышей наблюдают глубокую слабость и гипотонию, трудности контроля головы, слабый крик и кашель, трудности с глотанием и выведением мокроты, осложнённое течение ОРВИ, развитие дыхательной недостаточности, высокие риски аспирационной пневмонии, очень высокую скорость прогрессирования заболевания.
При II типе у ребёнка будет задержка моторного развития и набора веса, слабый кашель, тремор рук, контрактуры, сколиоз и деформация грудной клетки.
Отличительный признак СМА – заболевание может проявить себя не сразу, и до определённого возраста ребёнок будет развиваться абсолютно нормально. Затем происходит постепенная потеря всех приобретённых навыков. Поэтому СМА называют очень коварной болезнью.
Как диагностируют СМА?
СМА обычно диагностируют по клиническим симптомам и подтверждают с помощью генетического анализа.
Как лечат СМА?
Есть 3 препарата, которые применяются для лечения СМА.
В августе 2019 фармацевтическая компания Biogen зарегистрировала в России препарат «Спинраза», который вводят в спинной мозг один раз в несколько месяцев. Лечение пожизненное.
В ноябре 2020 года регистрационное удостоверение получил «Эврисди» (рисдиплам) от компании Roche. По принципу действия он похож на Спинразу, но выпускается в виде раствора для приёма в рот, поэтому его удобно применять в домашних условиях.
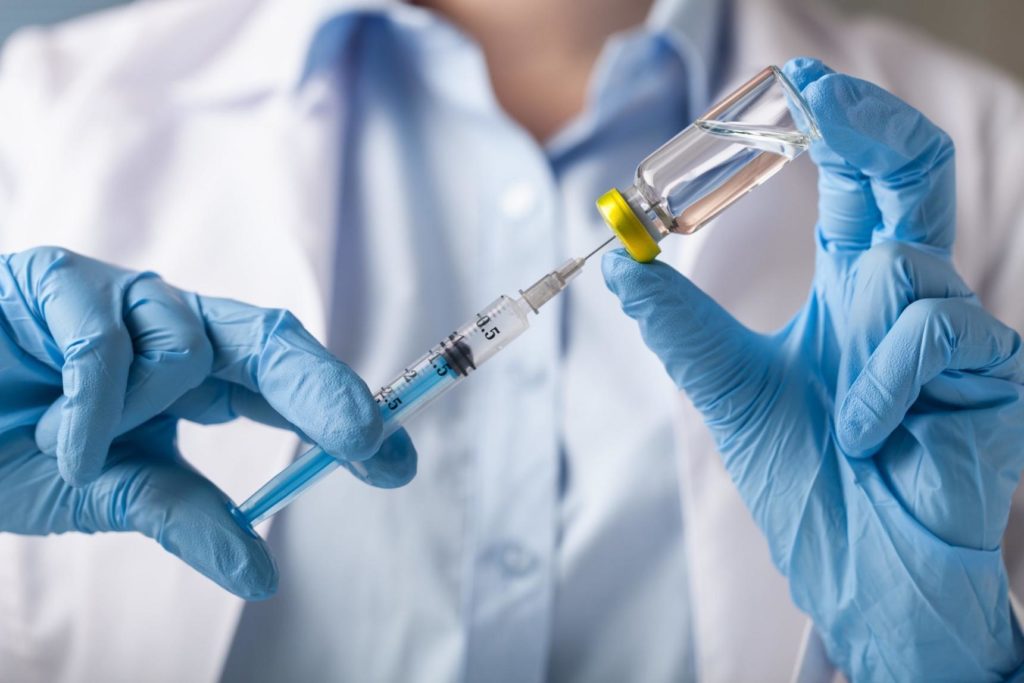
Самый известный и самый дорогой в мире препарат от СМА – «Золгенсма», изобретённый в 2019 году в США. Его принципиальное отличие в том, что он не просто приостанавливает прогрессирование болезни, а заменяет отсутствующий или дефектный ген, который отвечает за выработку белка SMN, на его функциональную копию. «Золгенсма» не просто приостанавливает развитие болезни, но и улучшает общее состояние, практически возвращая больного к обычной полноценной жизни.
Если поставить инъекцию вовремя, желательно до проявления клинических симптомов, ребёнок не будет отличаться от сверстников. В отличие от той же «Спинразы», которую нужно ставить несколько раз в год пожизненно, «Золгенсма» – это одноразовое лечение. Пока этот препарат не зарегистрирован в России. Его стоимость – около 155 миллионов рублей.
Почему инъекция «Золгенсма» такая дорогая?
Цена «Золгенсмы» прямо пропорциональна стоимости и сложности его разработки. Так, согласно исследованию 2016 года, опубликованному в Journal of Health Economics, для создания одного нового лекарства требуется в среднем 2,6 миллиарда долларов и больше 10 лет упорной работы. Эксперты отмечают: как и большинство революционных лекарств, цена «Золгенсмы» отражает высокую стоимость её разработки и ценность, которую она приносит, а не просто стремление к прибыли.
Кроме того, как мы уже говорили, препарат ставится всего 1 раз в жизни. А значит, в долгосрочной перспективе «Золгенсма» для пациента выгоднее пожизненной «Спинразы». Также причина дороговизны в том, что препарат ориентирован на очень малую группу больных – всего несколько тысяч на весь мир. Поэтому все затраты на разработку и тестирование лекарства ложатся, по сути, на их плечи.
Сколько людей в России имеют диагноз СМА?
По данным фонда «Семьи СМА», в России насчитывается около 3 000–5 000 людей с этим диагнозом. Ежегодно в нашей стране рождается примерно 200 детей со СМА.
Спинальная мышечная атрофия (СМА): что это такое?
Что такое СМА?
СМА (спинальная мышечная атрофия) ― генетическое нервно-мышечное заболевание, поражающее двигательные нейроны спинного мозга и приводящее к нарастающей мышечной слабости. Заболевание носит прогрессирующий характер, слабость начинается с мышц ног и всего тела и с развитием заболевания доходит до мышц, отвечающих за глотание и дыхание. При этом интеллект больных СМА абсолютно сохранен.
В зависимости от тяжести симптомов выделяют 3 основных типа проксимальной СМА: СМА 1, СМА 2, СМА 3. Чем раньше проявляются первые признаки болезни, тем ярче выражены симптомы, тем они тяжелее и тем быстрее прогрессирует заболевание.
СМА I (БОЛЕЗНЬ ВЕРДНИГА-ГОФФМАНА)
Наиболее тяжелая форма. Возраст проявления болезни: до 6 месяцев
СМА II (БОЛЕЗНЬ ДУБОВИЦА)
Возраст проявления болезни: 6-18 месяцев.
Описание
Юлия Самойлова. Самый известный в России человек со СМА. Фото: https://www.instagram.com/jsvok/
СМА III (БОЛЕЗНЬ КУГЕЛЬБЕРГА-ВЕЛАНДЕРА)
Возраст проявления болезни: после 18 месяцев
Механизм СМА
СМА вызывается поломкой в гене SMN1. Ген SMN2 частично компенсирует утрату гена SMN1.
Диагностика и помощь специалистов
При выявлении симптомов, которые могут указывать на болезнь, необходимо комплексное обследование для установления точного диагноза.
Диагностика: необходимо получить консультацию невролога, специалиста по нервно-мышечным заболеваниям, который может установить диагноз на основании симптомов. Для подтверждения диагноза требуется проведение ДНК-диагностики и консультация генетика.
Генетическая диагностика: тест ДНК для выявления делеции гена SMN1 и определения количества копий SMN2.
Дополнительные исследования:
Медицинская помощь
Врачи-специалисты:
Невролог ― ставит диагноз, назначает поддерживающее лечение, ведет постоянное наблюдение за ходом болезни.
Генетик ― ставит диагноз и, в случае необходимости, консультирует семью по вопросам дальнейшего потомства.
Участковый педиатр (терапевт) ― помогает лечить болезни, которыми болеют все.
Пульмонолог или реаниматолог ― помогает выявить и скомпенсировать дыхательные нарушения, решать проблемы с откашливанием, дает консультации по респираторной поддержке.
Ортопед ― оценивает нарушения опорно-двигательного аппарата (контрактуры, деформации), определяет необходимый объем профилактических мер, помогает корректировать эти нарушения.
Нейрохирург ― занимается исправлением сколиоза.
Физический терапевт ― подбирает комплекс упражнений и абилитационных процедур и обучает родителей регулярно делать их дома самостоятельно.
Нутрициолог или диетолог ― помогает подобрать оптимальное питание.
Гастроэнтеролог ― помогает в случае возникновения проблем с желудком и кишечником.
Кардиолог ― наблюдает за работой сердечно-сосудистой системы.
Специалист по паллиативной помощи ― помогает комплексно улучшить качество жизни.
Другие специалисты привлекаются по мере возникновения специфических проблем.
Помогающие организации
Благотворительный фонд «Семьи СМА» — единственная в России организация, специализирующаяся на помощи семьям, столкнувшимся со спинальной мышечной атрофией. Оказывается благотворительную, информационную, психологическую поддержку семьям, консультирует специалистов по вопросам заболевания и методов работы с пациентами со СМА.
Фонд помощи хосписам «Вера». Благотворительная и консультативная помощь семьям с неизлечимо больными детьми, неизлечимо больным взрослым.
ОДКБ № 1 Отделение паллиативной помощи детям, Екатеринбург, Свердловская область. Оказывается медицинскую, информационную, социальную и психологическую помощь семьям, воспитывающим ребенка-инвалида с паллиативным состоянием.
«Научно-исследовательский клинический институт педиатрии имени академика Ю.Е. Вельтищева» ФГБОУ ВО РНИМУ им.Н.И.Пирогова. Институт находится в Москве. Обращаться за медицинской помощью детям со СМА и другими нервно-мышечными заболеваниями могут жители всей России.
Клиника «Чайка». Консультации врача-пульмонолога Штабницкого Василия Андреевича для детей и взрослых со СМА.
Детский хоспис «Дом с маяком» (Москва, ближнее Подмосковье). Медицинская, психологическая, правовая, социальная, благотворительная помощь семьям с неизлечимо больными детьми и молодыми взрослыми (до 25 лет).
Марфо-Мариинский медицинский центр «Милосердие» (г.Москва). Медицинская, психологическая, правовая помощь, помощь няни, мероприятия, духовная поддержка, благотворительная помощь семьям с неизлечимо больными детьми.
Во второй части материала читайте о лечении СМА и помощи в зависимости от состояния пациента, а также о планировании потомства после того, как в семье родился ребенок со СМА.
Более подробную информацию вы найдете на сайте благотворительного фонда «Семьи СМА» и их специального проекта о жизни со спинальной мышечной атрофией. Спецпроект предназначен тем, кто столкнулся с диагнозом СМА и хотел бы узнать все самое важное об этой болезни: к каким специалистам и куда обращаться, как ухаживать, за чем следить, о чем помнить, какая терапия существует на сегодняшний день.
Как не пропустить у ребенка редкое генетическое заболевание
Почему у здоровых родителей рождаются дети с тяжелыми болезнями? Ответы стоит поискать в генетике. Например, каждый 40-й житель нашей планеты – здоровый носитель редкого генетического заболевания «спинальная мышечная атрофия» (СМА). В России каждый год рождается примерно 250-300 детей со СМА.
Наш эксперт Лолита Алиевна Пак — доктор медицинских наук, руководитель Центра редких болезней ФГАУ «НМИЦ здоровья детей» Минздрава России — рассказывает, можно ли «предугадать» рождение ребенка с генетическим заболеванием и как распознать первые симптомы болезни.
Что такое СМА
Спинальная мышечная атрофия (СМА) – редкое тяжелое наследственное заболевание. Причиной развития СМА являются мутации в гене SMN1 (ген выживаемости мотонейронов), который отвечает за синтез белка выживаемости мотонейронов (SMN). Мотонейроны, или двигательные нейроны, – это нервные клетки, передающие нервные импульсы от головного мозга к мышцам. При дефиците белка SMN в мотонейронах происходят необратимые процессы, которые в конечном итоге приводят к их гибели. В результате нервный стимул прекращает передаваться к мышцам и они атрофируются.
При прогрессировании заболевания ребенок утрачивает двигательные навыки: перестает держать голову, переворачиваться, самостоятельно сидеть, стоять и ходить. Слабость дыхательных мышц также приводит к развитию дыхательных нарушений.
Однако у людей есть еще и резервный ген SMN2, который схож с основным геном SMN1. Он производит около 10% нормального белка SMN и может уменьшить тяжесть течения заболевания.
Как минимизировать риски болезни
Если в семье оба родителя — носители редкого генетического заболевания, то при аутосомно-рецессивных заболеваниях, а СМА относится к их числу, в 25% случаев ребенок родится здоровым, в 50% — станет просто носителем мутации. Однако в 25% случаев существует риск рождения ребенка со СМА.
Если в семье уже есть ребенок со СМА или один из будущих родителей знает о том, что он является носителем заболевания, лучше заранее провести генетическое исследование.
Можно ли повлиять на этот риск? В целом это невозможно. Но если пара решит прибегнуть к процедуре ЭКO, то из нескольких эмбрионов можно будет выбрать здорового. Другой вариант – воспользоваться услугами донора, у которого нет этой генетической поломки. Также во время беременности можно провести пренатальную дигностику у плода, и если заболевание обнаружится, то следует обязательно проконсультироваться с врачом, чтобы обсудить дальнейшие шаги по ведению беременности.
Неонатальный скрининг (скрининг новорожденных)
Очень важно диагностировать СМА на самых ранних этапах. Недавно Правительство РФ объявило о планах расширения государственной программы неонатального скрининга до 36 нозологий. В настоящее время туда включены только 5 наследственных заболеваний: фенилкетонурия, муковисцидоз, врожденный гипотиреоз, aдреногенитальный синдром и галактоземия. Когда программа будет расширена, дети со СМА смогут быть диагностированы сразу после рождения – еще до возникновения клинических симптомов, что позволит назначить патогенетическое лечение и изменить течение болезни, предотвратив развитие осложнений.
В ряде регионов также запланированы пилотные проекты по неонатальному скринингу на спинальную мышечную атрофию и первичные иммунодефициты. Их старт ожидается уже в конце 2021 года.
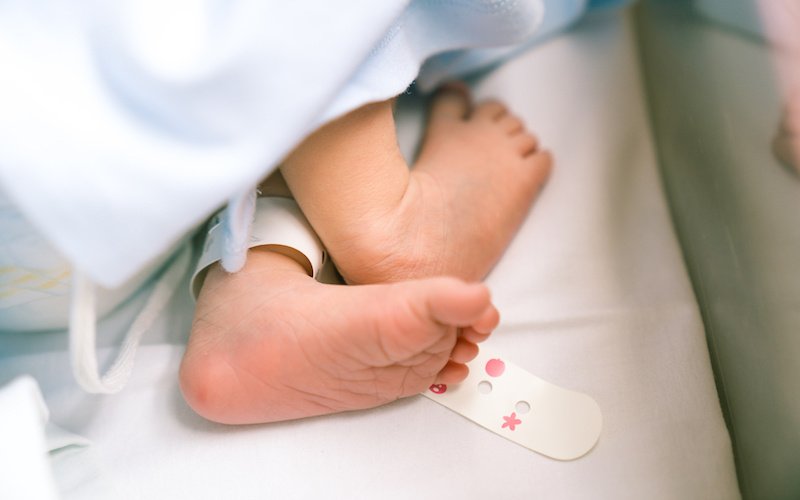
Обычно забор крови ребенка на неонатальный скрининг осуществляется в роддоме с использованием специальных тест-бланков. Затем образцы направляются в медико-генетическую лабораторию — и результат становится известен уже через несколько дней. Такой тест, добавленный в рутинный скрининг, не потребует никаких дополнительных медицинских манипуляций.
Если в вашем родильном доме предлагают сделать ребенку тест на СМА, обязательно соглашайтесь!
Значение имеет каждый день: первые симптомы СМА
Спинальная мышечная атрофия очень быстро прогрессирует — значение имеет буквально каждый день. Важно заметить ее признаки как можно раньше, чтобы ребенок быстрее получил помощь. В зависимости от того, в каком возрасте появились симптомы заболевания, различают несколько типов СМА.
Самый тяжелый тип – СМА I типа. Клинические симптомы заболевания могут появиться от рождения до 6 месяцев жизни ребенка.
Для СМА I типа характерны синдром «вялого ребенка», мышечная слабость, задержка двигательного развития – ребенок плохо удерживает голову, не активно двигает руками и ногами. У этих детей всегда присутствуют нарушения дыхания и глотания. Часто возникают контрактуры – ограничение пассивных движений в суставе. Обычно они проявляются в коленных и лучезапястных суставах, реже – в локтевых. Нарушение глотания может приводить к aспирационной пневмонии (воспалению легких, возникающему из-за попадания в них слюны, содержимого желудка и других инородных веществ) и летальному исходу. Большинство детей со СМА I типа без постоянного ухода и медицинского сопровождения погибает в возрасте до двух лет.
СМА II типа проявляется позднее — в возрасте 7-18 месяцев — и протекает менее тяжело. Дети сохраняют способность удерживать голову самостоятельно, сидеть, но никогда не овладевают навыком ходьбы. При СМА II типа ноги и руки ребенка выглядят ослабленными и вялыми, ему трудно долго удерживаться в сидячем положении, стоять. Малыш может раскачиваться из стороны в сторону, но не может полностью перевернуться на бок. Заметны незначительный тремор или подергивания пальцев вытянутых рук. Приобретенные ранее навыки могут постепенно теряться. Часто возникают трудности при кашле, развиваются и прогрессируют скелетные деформации (выраженный сколиоз, суставные контрактуры). Около 70% пациентов доживают до возраста 25 лет.
Спинальная мышечная атрофия: что это такое и как ее вылечить
О спинальной мышечной атрофии у детей говорят все чаще, обычно — в контексте появления долгожданных лекарств против нее. Можно ли спасти всех больных и что для этого требуется?
Что такое СМА?
Спинальная мышечная атрофия (СМА) — это целая группа наследственных, генетических заболеваний, при которых страдают двигательные нейроны передних рогов спинного мозга. Из-за мутации в гене SMN1 у больных СМА снижена выработка SMN-белка, без которого нейроны разрушаются и перестают передавать сигналы от мозга к мускулатуре. В результате у человека постепенно атрофируются мышцы конечностей, головы и шеи.
Какой тип СМА самый опасный?
Существует 5 основных типов спинальных мышечных атрофий. Каждый из них имеет свои особенности, в том числе – симптомы и время манифестации.
Во многом тяжесть и скорость развития болезни определяется количеством у ребенка копий гена SMN2, он почти идентичен гену SMN1 и может в некоторой степени компенсировать его поломку.
Высокая смертность в случае отсутствия раннего лечения характерна только для СМА нулевого и первого типов. Большая часть пациентов с другими типами атрофий доживает до взрослого возраста. Четвертый тип, затрагивающий взрослых, на продолжительность жизни значительного влияния не оказывает.
Почему именно я? Как часто врачи ставят страшный диагноз
Обычно тип наследования СМА у детей — аутосомно-рецессивный. Некоторые, более редкие виды СМА, имеют другой тип наследования, а могут вообще не передаваться следующим поколениям. Это значит, что ребенок может заболеть только в том случае, если у обоих родителей есть поломанный ген, ответственный за синтез соответствующего белка. И даже тогда вероятность болезни составляет лишь 25%. Еще в четверти случаев ребенок вообще не унаследует мутаций, и в половине — сам станет бессимптомным носителем.
Согласно последним данным, в среднем дефектные гены, вызывающие мышечную атрофию, можно найти у каждого пятидесятого новорожденного, что не так мало, как хотелось бы. Сегодня среди 10 тысяч младенцев СМА диагностируют хотя бы у одного. Не зря эта болезнь является одной из ведущих причин детской смертности, связанных с генетическими нарушениями.
Когда стоит заподозрить неладное? Симптомы болезни
СМА первого типа может стать заметна почти сразу после рождения. Младенцы с этой тяжелой патологией:
Дети с СМА первого типа сначала могут выглядеть совершенно здоровыми. Однако со временем родители замечают, что ребенок мало двигается, быстро набирает вес, ему все труднее держать игрушки. Так как начинать лечить мышечную атрофию нужно как можно раньше, появление любых описанных симптомов — повод немедленно обратиться к врачу-неврологу.
Дети с СМА второго типа начинают отставать в развитии после 6–7 месяцев. Симптомы могут развиться еще позже, но обычно — до достижения ребенком 18 месяцев жизни. Дети с этой формой спинальной атрофии:
СМА третьего типа возникает к 1,5–2 годам, иногда — в позднем детстве или в подростковом возрасте. Ее основные признаки:
Взрослые, столкнувшиеся с СМА четвертого типа, как правило, жалуются на:
Эта форма СМА также способна прогрессировать, но почти никогда не затрагивает мускулатуру, отвечающую за дыхание, а потому не составляет угрозы жизни.
Может ли болезнь пройти сама по себе?
СМА — это расстройство, вызванное специфической мутацией в геноме. Оно всегда имеет прогрессирующий характер и не может пройти со временем, так как наша ДНК не способна починить сама себя, избавившись от нежелательных элементов кода.
Лечение СМА. Спинраза — это единственная надежда?
До недавнего времени вылечить СМА было невозможно, и все действия сводились к поддержанию жизни и улучшению ее качества. Для этого, например, используются специальные упражнения и приборы, призванные помочь двигаться и дышать, в том числе — зонды для кормления.
Настоящим прорывом стала разработка первого эффективного лекарства против спинальной мышечной атрофии. Препарат Спинраза (нусинерсен) был одобрен в США в 2016 году, а в России — в 2019-м. Он направлен на лечение всех типов СМА и подходит для пациентов всех возрастов. В основе — небольшие последовательности нуклеотидов, позволяющих синтезировать белок SMN на базе другого, схожего гена в нашей ДНК — SMN2. Препарат вводят в спинномозговую жидкость. Одной инъекции недостаточно. Чтобы защитить нейроны, лекарство нужно использовать регулярно: несколько раз в первый год жизни, и каждые 4 месяца — после.
В прошлом году в России стал доступен Рисдиплам. Он, как и Спинраза, воздействует на прочтение гена SMN2, но его можно пить в виде таблеток, что гораздо удобнее.
Третий препарат против СМА — Золгенсма (онасемноген абепарвовек), в нашей стране пока не зарегистрирован. Его применяют у детей до 2 лет. Внутри лекарства — аденовирусный вектор (оболочка вируса), который доставляет в нейроны работающий ген SMN1, после чего клетки начинают синтезировать нужный им белок (ДНК ребенка при этом никак не изменяется). Так как это средство генной терапии, для полного выздоровления хватает всего лишь одной дозы лекарства, в чем его значительное преимущество.
Сколько стоит лечение и когда его не поздно начать?
Ситуация для больных детей усугубляется в связи с тем, что лечить СМА нужно на ранних стадиях, так как из-за болезни нейроны отмирают постоянно, день за днем. Если ребенок болен СМА первого типа, у него есть в запасе около двух лет, у маленьких пациентов с другими формами болезни времени для лечения чуть больше, но прогноз тем лучше, чем раньше начата терапия. И все же на сегодняшний день прогресс в лечении СМА очевиден. Этот диагноз – больше не приговор, а в будущем спасительные лекарства, несомненно, будут становиться все эффективнее и дешевле.
Почему у людей бывает СМА?
Спинальная мышечная атрофия – это заболевание, при котором повреждается ген SMN1. В результате мутации у человека не вырабатывается белок, который нужен для выживания мотонейронов. Мотонейроны — важная часть спинного мозга человека, от них по длинным нервам идут сигналы к скелетным мышцам организма. Если мотонейрон получает недостаточно белка для своего питания, то он быстро устает. Ему приходится работать и за себя, и «за того парня». Многие мотонейроны просто гибнут от «усталости», — нагрузка на оставшиеся возрастает, и в результате они работают с чудовищной перегрузкой. От усталости они не могут посылать сигналы к скелетным мышцам, благодаря которым человек ходит, сидит, лежит, глотает или дышит. Мышцы остаются без работы, потому что их никто ничего не просит сделать, и постепенно отмирают.
Дефицит важного белка, который не вырабатывает ген SMN1, приводит к атрофии (потере жизнеспособности и уменьшению размера) мышц, и в результате человек постепенно теряет способность ходить, удерживать и управлять собственным телом, самостоятельно сидеть, есть, глотать и дышать. Упрощенный механизм СМА можно увидеть на схеме.
К счастью, у человека есть еще ген SMN2, который дублирует SMN1. Он производит нефункциональный белок и небольшое количество нормального белка, который позволяет мотонейронам человека выживать на очень голодном пайке. В результате человек со СМА сохраняет какую то часть своих двигательных, глотательных и дыхательных функций.