На чем основана комплексонометрия
На чем основана комплексонометрия
В анализе используют ее динатриевую соль Na2H2L ∙ 2Н2О, которая в отличие от кислоты хорошо растворима в воде и находит более широкое применение:
комплексон ІІІ (трилон Б, ЭДТА, динатрия эдетат)
В растворе трилон Б диссоциирует на ионы:
Во всех случаях независимо от степени окисления катионов они реагируют с комплексоном в соотношении 1: 1, поэтому фактор эквивалентности для ЭДТА и катионов металла равен 1.
Схематически реакции комплексообразования с катионами, имеющими различные степени окисления, можно представить следующими уравнениями:
В качестве титранта используют растворы 0,1; 0,05 или 0,02 моль/дм 3 трилона Б.
При этом комплекс катиона с индикатором и свободный индикатор имеют различную окраску:
(окраска 1) (окраска 2)
При комплексонометрическом титровании к анализируемому раствору прибавляют металлоиндикатор, который образует с определяемыми катионами комплекс, имеющий определенную окраску. В процессе титрования трилоном Б комплекс катионов металла с индикатором разрушается и образуется бесцветный, очень прочный комплекс катионов с трилоном Б, а в раствор переходят ионы свободного индикатора:
(окраска 2) (окраска 1)
Конечную точку титрования определяют по собственной окраске индикатора (окраска 1).
Условия комплексонометрическоro титрования:
1. Реакции комплексообразования должны протекать быстро, количественно и стехиометрично, чтобы вблизи точки эквивалент-ности определяемые катионы были практически полностью связа-ны в комплекс. Константа нестойкости образующихся комплексов должна быть малой величиной.
2. Определяемые ионы должны образовывать с металлоиндиктором менее прочные комплексы, чем их комплексы с трилоном Б.
3. Комплексонометрическое титрование следует проводить при определенном значении рН (рН
Очень прочные комплексы с комплексоном III образуют катионы Fe 3+ Sn 2+ и другие, их можно определить в кислой среде. Катионы, образующие менее прочные комплексы с трилоном Б, не мешают определению, так как не титруются в кислой среде.
Способы комплексонометрического титрования.
Обратное титрование. К анализируемому раствору прибавляют аммиачный буферный раствор, затем точно отмеренный удвоенный минимальный объем (35,00-40,00 см 3 ) стандартного раствора трилона Б, который вступает в реакцию с определяемыми ионами, а его избыток оттитровывают стандартным раствором магния сульфата или цинка сульфата в присутствии металлоиндикатора. При этом протекают реакции:
изб. H2L 2- + Zn 2+ ↔ [ZnL] 2- + 2Н +
Способ обратного титрования применяют:
· когда реакция комплексообразования протекает медленно;
· нет подходящего индикатора для фиксирования конечной точки титрования при прямом способе титрования;
· индикатор образует с определяемым ионом очень прочный комплекс, который не разрушается комплексоном;
· для определения катионов в нерастворимых в воде осадках например Са 2+ в СаС2О4, Mg 2+ в MgNH4PО4, Рb 2+ в PbSО4 Заместительное титрование. Метод основан на том, что большинство ионов образуют с трилоном Б более устойчивые комплексные соединения, чем комплекс катионов Mg 2+ с трилоном Б [MgL] 2- (β = 9,72). После прибавления к анализируемому раствору комплекса [MgL] 2- протекает реакция обмена:
[MgL] 2- + Ме 2+ → [MeL] 2- + Mg 2+
Эта реакция возможна потому, что ионы металла образуют с H2L 2- более прочное комплексное соединение [MeL] 2- (β > 9,2), и равновесие вышеприведенной реакции смещается вправо. Выделившиеся ионы Mg 2+ оттитровывают стандартным раствором трилона Б в присутствии металлохромного индикатора:
Трилонометрическим методом определяют:
а) общую жесткость воды;
б) практически все катионы щелочноземельных и тяжелых металлов;
Комплексонометрическое титрование
Титратор для комплексонометрического титрования. GT-200
Чтобы унифицировать получаемые результаты анализа и избежать индикаторной ошибки рекомендуется применять автоматизированные установки. Они позволят выполнять анализ в строго контролируемых одинаковых условиях, фотометрически детектируя смену окраса раствора.
Комплектация автоматического лабораторного титратора для комплексонометрического титрования на примере модели GT-200 от японской компании “Mitsubishi Chemical Analytech Co., Ltd.” (с 2020 года перешла в собственность «Nittoseiko Analytech»):
Основной блок – потенциометрический титратор GT-200 – управляется либо встроенным программным обеспечением, либо с помощью WINDOWS-совместимого ПО. Он производит все расчетные операции и сохраняет необходимые данные (концентрации, объемы, статистику и пр.) в памяти.
Бюретка для титрования GT-200BRT – предназначена для дозирования и титрования растворов. Можно задавать шаг, скорость, последовательность дозирования.
Фотометрический датчик GT-LDII – имеет встроенный детектор, вырабатывающий фототок при определенной длине волны. При смене окраса раствора длина волны меняется, изменяя фототок. В процессе подачи титранта объем поданного раствора можно зафиксировать до смены окраса индикатора и после.
Мешалка GT-200STR – позволяет производить контролируемое и повторяемое перемешивание пробы.
Это основные элементы автоматической системы для фотометрического титрования на базе потенциометрического титратора GT-200. Дополнительно к ним можно добавить устройства для автоматической подачи образцов, принтер для распечатки результатов, весы с возможностью передачи веса образца сразу в прибор и другие полезные модули.
Сущность комплексонометрического титрования
Комплексонометрическое титрование – это титриметрический метод анализа, основанный на взаимодействии определяемых ионов металла с комплексонами. Чаще всего в роли комплексообразователя выступает динатриевая соль этилендиаминтетрауксусной кислоты (другие названия: Трилон Б, ЭДТА), которая в большинстве случаев образует комплексы с катионами металлов в молярном соотношении 1:1, что упрощает расчет концентраций определяемых элементов.
Устойчивые комплексы с ЭДТА большинство металлов образуют в щелочной среде, для этого к раствору с анализируемым образцом добавляют аммиачный буфер, но некоторые элементы, например, железо (Fe III), можно титровать и в кислой среде.
Основные требования к комплексообразующему реагенту:
Образования устойчивых комплексов с катионами металлов в известном молярном соотношении.
Хорошая растворимость образуемых комплексов в воде.
Образующиеся комплексы не должны быть окрашены.
Взаимодействие комплексона с противоионом должно происходить быстро и количественно
Всем этим требованиям, в большинстве случаев, удовлетворяет Трилон Б.
Индикатор подбирают в зависимости от титруемого элемента и исходя из типа титрования.
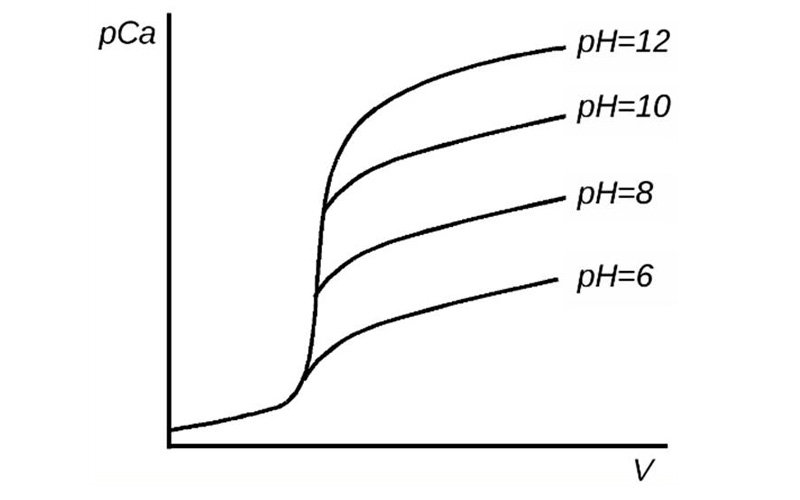
Как уже упоминалось ранее, pH среды существенно влияет на устойчивость образующихся комплексов, что видно при построении кривой комплексонометрического титрования ионов кальция, представленной ниже:
Рис.1 Кривая титрования [Ca 2+ ] трилоном Б при различных значениях pH.
Из кривых титрования видно, что при более высоком pH величина ΔpCa больше (высокий скачок), что позволяет точней идентифицировать точку эквивалентности.
Классификация методов комплексонометрического титрования
Как и большинство титриметрических методов, комплексонометрию можно проводить прямым, обратным или заместительным титрованием.
В случае прямого титрования первоначальное окрашивание раствора вызвано взаимодействием индикатора с металлом. В дальнейшем сильный комплексообразователь трилон Б вытесняет индикатор, образуя с металлом более устойчивый комплекс. В ходе этого взаимодействия наблюдается смена цветности раствора. Титрант добавляется до получения устойчивого окраса, что говорит о присутствии в растворе свободного Трилона Б.
Обратный метод титрования подразумевает добавление избытка комплексона к раствору. Непрореагировавшую часть ЭДТА оттитровывают солью цинка или магния. Зная первоначально добавленный объем ЭДТА и вычтя из него количество оттитрованного избытка, можно вычислить содержание металла, вступившего во взаимодействие с комплексоном. Этот способ предпочтителен для элементов, которые медленно взаимодействуют с Трилоном Б, для которых сложно подобрать индикатор. Металлы в нерастворимых в воде солях тоже определяют обратным титрованием. Кроме того, если индикатор образует более прочный комплекс с металлом, чем титрант, то обратное комплексонометрическое титрование поможет определить его содержание.
При заместительном титровании к образцу добавляют комплексы металлов, которые легко вытесняются определяемыми металлами в образце. Избыток добавленного раствора оттитровывается стандартным раствором ЭДТА.
Комбинированные методы комплексонометрического титрования
Виды комплексонометрического титрования
Различают комплексонометрические методы в зависимости от используемого хелата:
Трилон Б – трилонометрия. Обычно применяется для определения катионов металлов.
Соединения ртути – меркуриметрия. Применяется для анализа анионов (галогенов, цианидов и пр.).
Фосфорорганические комплексоны. Применяются относительно недавно и позволяют специфично определять катионы металлов даже в смесях.
Можно классифицировать методы комплексонометрического титрования в зависимости от используемого индикатора.
Индикаторы для комплексонометрического титрования
Также в комплексонометрическом титровании используют такие индикаторы, как: Пирокатехиновый фиолетовый, Мурексид, кальцес, Хромовый темно¬синий, Бериллон II, Кальцион, Кальцеин и пр.
При индикаторном титровании необходимо четко фиксировать смену окраса индикатора для определения конечной точки титрования. Учитывая особенности индивидуального цветовосприятия, момент перехода окраса у разных лаборантов может отличаться, что влияет на точность получаемых результатов, повторяемость.
Применение комплексонометрического титрования
Методы комплексонометрического титрования особенно важны при определении Ca и Mg при анализе воды на жесткость (ГОСТ 52407-2005, ГОСТ 4151-72, ПНД Ф 14.1:2.98-97 и др. методики). Эти показатели определяют ее целевое назначение и пригодность для бытового и технологического использования. Кроме этого существуют внутренние нормативные документы на предприятиях, которые регулируют качество используемой воды и методы ее анализа.
Методики определения других элементов востребованы в различных отраслях химической промышленности. Эти задачи решаются титрованием. В ГОСТ 10398-2016 представлены методы анализа для широкого перечня элементов в составе реактивов и особо чистых веществ.
Комплексонометрия: сущность метода, общая характеристика, область применения. Металл – индикаторы, механизм их действия
Комплексонометрия – метод количественного титриметрического анализа, основанный на образовании комплексных соединений ионов металлов с комплексонами.
Комплексонами называют органические соединения, молекулы которых содержат как кислотные, так и основные группы и потому способные образовывать с ионами металлов внутрикомплексные соединения.
Внутрикомплексные соединения образуются в тех случаях, когда ионы металла-комплексообразователя с одной стороны замещают активные ионы водорода кислотных функциональных групп, а с другой стороны образуют связь по донорно-акцепторному механизму за счет свободных орбиталей иона металла и атомов основных групп, имеющими неподеленные электронные пары.
К числу функциональных групп, содержащих ионы водорода, способные замещаться ионами металла-комплексообразователя, относятся: −COOH, −OH, −SO3H, −NH2, −SH, =NH.
К числу функциональных групп, с которыми ионы металла-комплексообразователя способны образовывать связь по донорно-акцепторному механизму, относятся: ≡N, =NH, −NH2, −OH, =C=O, − S −, −N=N−.
В практике химического анализа как правило используют аминополикарбоновые кислоты или их соли.
Чаще всего в качестве комплексона используют ЭДТА (двузамещенный этилендиаминтетраацетат натрия)
| ЭДТА; комплексон III; трилон Б; H2Na2Y; H2Y 2- |
При взаимодействии с ЭДТА ион металла замещает ионы водорода карбоксильных групп и образует координационную связь за счет неподеленных электронных пар атомов азота и свободных орбиталей иона металла. При этом образуется хелатный комплекс с тремя пятичленными циклами. Схематично эту реакцию можно выразить уравнением:
Однако показанный на схеме реакции комплекс в действительности имеет следующее строение:
При титровании ЭДТА солей металлов-комплексообразователей протекают следующие реакции:
1) диссоциация комплексона:
Na2H2Y 
2) взаимодействие с металлами:
Me 2+ (Ca 2+ ) + H2Y 2− 
Me 3+ (Al 3+ ) + H2Y 2− 
Me 4+ (Th 4+ ) + H2Y 2- 
Реакции с участием комплексонов протекают стехиометрично, образуются очень прочные комплексы с соотношением металла к лиганду 1:1 не зависимо от заряда иона металла.
При проведение комплексонометрического определения необходимо соблюдать определенные условия, важнейшим из которых является рН раствора. В сильно кислых растворах (рН 10 происходит образование малоустойчивых оксокомплексов или гидрооксиды Ме.
Из выше приведенных реакций следует, что образование комплексонатов происходит с выделение кислоты, что приводит к увеличению рН.
Поэтому, как правило, титрование проводят в присутствии соответствующих буферных растворов поддерживающих рН на определенном уровне.
В комплексонометрии используют методы прямого и обратного титрования, а также метод замещения.
Метод обратного титрования.В тех случаях, когда по тем или иным причинам невозможно провести прямое титрование, используют обратное титрование. К анализируемому раствору прибавляют точно измеренный объем стандартного раствора комплексона, нагревают до кипения для завершения реакции комплексообразования, а после охлаждения оттитровывают избыток комплексона стандартными растворами MgSO4 или ZnSO4. Этот метод применяют в тех случаях, когда нет подходящего индикатора, когда в буферном растворе выпадает осадок гидроксида металла и когда реакция комплексообразования протекает медленно. Методом обратного титрования также определяют содержание катионов в нерастворимых в воде соединениях (Ca 2+ в CaC2O4, Mg 2+ в MgNH4PO4, Pb 2+ в PbSO4 и т.п.).
Th 4+ + MgY 2− 
Mg 2+ + H2Y 2− 
Выбор индикатора для комплексонометрии осуществляется с помощью кривых титрования. При этом кривую титрования строят по аналогии с кривыми для кислотно-основного титрования, откладывая на оси ординат значение рМ= − lg [M n + ], а на оси абсцисс – количество добавленного комплексона или процент титрования. При постепенном прибавлении раствора ЭДТА к раствору соли металла происходит уменьшение концентрации свободных ионов металла, вблизи точки эквивалентности наблюдается её резкое уменьшение − скачок титрования.
Величина скачка титрования имеет большое значение: чем он больше, тем легче установить конечную точку титрования. Величина скачка зависит от природы иона металла, устойчивости образующегося комплекса (чем устойчивее комплексонат, тем больше скачок), рН среды и концентрации растворов.
Как правило, для фиксирования точки конца титрования в комплексонометрии используют так называемые металл-индикаторы, которые представляют собой органические красители, образующие с катионами определяемых металлов растворимые в воде окрашенные комплексные соединения. Получаемые при этом комплексы менее устойчивы, чем комплексы металлов с комплексонами.
При добавлении индикатора к раствору соли металла образуется комплекс металла с индикатором, окрашенный определенным образом.
При титровании ЭДТА полученного раствора, малоустойчивый комплекс металла с индикатором разрушается и образуется более устойчивый неокрашенный комплекс металла с комплексоном, а индикатор выделяется в свободном виде, и в конечной точке раствор приобретает окраску, свойственную индикатору.
Этот ион проявляет себя как кислотно-основной индикатор. В зависимости от рН раствора индикатор существует в трех окрашенных формах: при рН 11,5 – желто-оранжевого:
В молекулу индикатора входят две фенольные группы и хромофорная азогруппа. Поэтому эриохром черный Т способен реагировать с ионами металла-комплексообразователя с образованием комплексных соединений.
В нейтральной и слабощелочной среде этот индикатор образует с большинством ионов металлов комплексы красного цвета следующего состава:
Сущность действия металл-индикатора на примере эриохрома черного Т можно представить следующим образом:
1) при добавлении индикатора к раствору соли металла (рН=8−10) образуется комплекс металла с индикатором красного цвета:
Me 2+ + HInd 2− 
2) при титровании полученного раствора ЭДТА этот комплекс разрушается, образуется более устойчивый бесцветный комплекс металла с комплексоном, а индикатор выделяется в свободном виде, придавая раствору синюю окраску:
MeInd − + Na2H2Y 
красный б/цв. б/цв. синий
Для поддержания рН раствора на требуемом уровне обычно в титруемый раствор добавляют аммиачную буферную смесь.
Индикаторы подбираются таким образом, чтобы интервал перехода их окраски находился в пределах скачка титрования. В настоящее время известно около 150 металл-индикаторов.
Кроме металл-индикаторов для фиксирования точки конца титрования в комплексонометрии используют обычные кислотно-основные индикаторы, так как реакция комплексообразования сопровождается выделением ионов водорода H + в количестве, эквивалентном количеству определяемого катиона. Выделившуюся кислоту определяют методом нейтрализации с обычными кислотно-основными индикаторами.
Окислительно-восстановительное титрование: сущность и методы. Окислительно-восстановительный потенциал и направление окислительно-восстановительных реакций. Фиксирование точки конца титрования в методах окислительно-восстановительное титрование. Редокс – индикаторы и требования к ним.
Методы окислительно-восстановительного титрования, или редокс-методы основаны на реакциях окисления – восстановления, связанных спереходом электронов от одних атомов, ионов или молекул к другим. Вещество, атомы, ионы или молекулы которого отдают электроны, окисляется и является восстановителем; вещество, атомы, ионы или молекулы которого принимают электроны, восстанавливается и является окислителем. Схематически это может быть выражено следующими уравнениями:
где Вос – восстановленная форма; Ок – окисленная форма.
Восстановленная форма одного вещества Вос1, отдавая электроны, переходит в окисленную форму Ок1 того же вещества. Обе эти формы образуют одну редокс-пару Ок1 /Вос1.
Окисленная форма Ок2 второго вещества, участвующего в окислительно-восстановительной реакции, принимая электроны, переходит в восстановленную форму Вос2 того же вещества. Обе эти формы также образуют редокс-пару Ок2 /Вос2.
В любой окислительно-восстановительной реакции участвуют, по крайней мере, две редокс-пары.
Методы окислительно-восстановительного титрования классифицируются по характеру основного титранта:
– перманганатометрия (основан на реакциях окисления восстановителей перманганатом калия KMnO4),
– хроматометрия (основан на реакциях окисления восстановителей дихроматом калия K2Cr2O7),
– йодометрия (основан на реакциях окисления восстановителей свободным йодом или на восстановлении окислителей йодидом калия KI) и др.
Достоинства метода окислительно-восстановительного титрования
1. Методы отличаются большой точностью и хорошей воспроизводимостью результатов.
2. Многие методы характеризуются быстротой выполнения и могут быть использованы для автоматического контроля.
3. Методы отличаются большим разнообразием, с их помощью можно определять не только окислители и восстановители, но и вещества, не проявляющие окислительно-восстановительных свойств.
4. Точку эквивалентности можно фиксировать с помощью индикаторов, а
также безиндикаторными и инструментальными методами.
5. Определения можно проводить прямым или обратным титрованием, а также методами замещения.
6. Многие окислители и восстановители легко получить в химически чистом виде, поэтому их титрованные растворы готовят по точной навеске. Приготовленные растворы можно использовать как для титрования, так и для стандартизации других растворов.
7. Титрование окислителями и восстановителями можно осуществлять во всех средах.
О/В потенциалы. Направление о/в реакций
Окислители и восстановители различаются по своей силе, т.е. по химической активности. Сила окислителей и восстановителей определяется величиной их стандартного окислительно-восстановительного потенциала.
Стандартным называется окислительно-восстановительный потенциал системы с концентрацией (активностью) окисленной и восстановленной форм равными 1 моль/л и измеренный по отношению к стандартному водородному электроду, потенциал которого принят равным нулю.
Чем больше стандартный окислительно-восстановительный потенциал данной пары, тем более сильным окислителем является окисленная форма и тем более слабым восстановителем ― восстановленная форма.
2Fe 3+ + Sn 2+ = 2Fe 2+ + Sn 4+
Стандартные окислительно-восстановительные потенциалы дают представление о возможном направлении окислительно-восстановительных реакций, но в реальных условиях это направление может быть иным.
В процессе окислительно-восстановительного титрования наблюдается изменение окислительно-восстановительных потенциалов взаимодействующих друг с другом систем.
Зависимость окислительно-восстановительного потенциала от концентраций окисленной и восстановленной форм выражается уравнением Нернста:

где E –окислительно-восстановительный потенциал пары, В;
E 0 – стандартный окислительно-восстановительный потенциал пары, В;
R – универсальная газовая постоянная (8,314 Дж/моль∙К);
n – число электронов, отданных или принятых одним атомом, ионом или
F – постоянная Фарадея (96500 Кл/моль);
[Ок] и [Вос] – концентрации соответственно окисленной и восстановленной форм, моль/л;
a и b – стехиометрические коэффициенты окислительно-восстановительной реакции.
Если подставить значения R, F, T = 298 K и перейти от натурального логарифма к десятичному, уравнение Нернста принимает вид:

уравнение Нернста имеет вид:

Если стандартные окислительно-восстановительные потенциалы взаимодействующих пар относительно близки, то изменяя концентрации окисленной и восстановленной форм можно изменить направление реакции на противоположное.
2Fe 3+ + 2I − ↔ 2Fe 2+ + I2 (1.4)
В присутствии NaF ионы Fe 3+ связываются в довольно прочный комплекс:
Однако если стандартные окислительно-восстановительные потенциалы взаимодействующих пар значительно отличаются друг от друга, никаким изменением концентраций нельзя изменить направление реакции на противоположное.
Например, Е 0 (Fe 3+ /Fe 2+ ) = 0,77В, Е 0 (MnO4 − /Mn 2+ ) = 1,51 В
5Fe 2+ + MnO4 − + 8H + = 5Fe 3+ + Mn 2+ + 4H2O
Реакцияможет протекать только в прямом направлении.
Константа равновесия о/в реакций
Возможность изменения направления окислительно-восстановительных реакций свидетельствует об их обратимости. В обратимых реакциях устанавливается химическое равновесие, которое характеризуется константой равновесия. Для реакции
2Fe 3+ + Sn 2+ ↔ 2Fe 2+ + Sn 4+
выражение константы равновесия имеет вид:

Окислительно-восстановительный потенциал системы в любой момент реакции может быть вычислен по одной из формул:


(Е 0 (Fe 3+ /Fe 2+ ) = 0,77В, Е 0 (Sn 4+ /Sn 2+ ) = 0,15В).
Когда потенциалы становятся равными, переход электронов от восстановителя к окислителю прекращается и в системе наступает равновесие. Тогда Е (Fe 3+ /Fe 2+ ) = Е (Sn 4+ /Sn 2+ ) и


Выражение 

подставим в формулу (1.7) и проведем преобразования:


Под знаком логарифма получили константу равновесия. Таким образом, для любой окислительно-восстановительной реакции

Из формулы (1.8) видно, что константа равновесия тем больше, чем больше разность потенциалов обеих пар, и если она велика, реакция идет практически до конца.
Фиксирование ТКТ в методах о/в титрования
Для фиксирования точки конца титрования в методах окислительно-восстановительного титрования широко применяются физико-химические (инструментальные) методы (потенциометрический, амперометрический, кондуктометрический, спектрофотометрический и др.). Из химических методов фиксирования точки конца титрования, можно выделить три основных способа.
Без индикатора можно также титровать восстановители раствором йода, т.к. при этом его бурая окраска исчезает, и одна лишняя капля раствора I2 окрасит раствор в бледно-желтый цвет. Однако, в этом случае результаты могут получиться менее точными, т.к. в интенсивность окраски от одной лишней капли йода меньше, чем для KMnO4.
Безиндикаторное титрование применимо в тех случаях, когда окраска окисленной и восстановленной форм резко отличается и если в растворе отсутствуют другие окрашенные вещества.
2. Использование специфических индикаторов.Это вещества, специфически реагирующие с одной из форм окислительно-восстановительной пары с изменением окраски.
В методах, основанных на титровании стандартным раствором йода или на выделении I2, точку эквивалентности устанавливают при помощи специфического индикатора – крахмала, образующего с йодом комплексно-адсорбционное соединение синего цвета. При титровании восстановителей раствором йода в присутствии крахмала, одна лишняя капля раствора I2 вызовет появление синей окраски, если же титруют восстановителем раствор йода, то в конечной точке синее окрашивание исчезает.
В некоторых случаях конец титрования определяют по обесцвечиванию красной окраски тиоцианата железа (III) Fe(SCN)3 в присутствии избытка восстановителя.
Эти способы фиксирования точки эквивалентности находят ограниченное применение.
3. Использование окислительно-восстановительных или редокс-индикаторов.Это вещества, которые изменяют свою окраску в зависимости от окислительно-восстановительного потенциала системы. Как правило, редокс-индикаторы представляют собой органические вещества, способные обратимо окисляться и восстанавливаться, и у которых окисленная и восстановленная формы имеют разную окраску. Схематично это можно представить следующим образом:
где Ind(ok) – окисленная, Ind(воc) – восстановленная форма индикаторов; n – число электронов, принимающих участие в окислительно-восстановительном процессе.
Потенциал такой индикаторной системы может быть рассчитан по уравнению Нернста:

где Е 0 – стандартный потенциал данной пары, когда [Ind(ок)] = [Ind(вос)].
Если к раствору восстановителя (окислителя) добавить 1-2 капли индикатора, то он окрасится определенным образом. При титровании этого раствора окислителем (восстановителем) отношение [Ind(ок)] / [Ind(вос)] будет меняться, но изменение окраски раствора будет заметно, когда концентрация одной из форм в 10 раз превысит концентрацию другой. Интервал перехода окраски индикатора будет определяться следующим образом:
К редокс-индикаторам относятся дифениламин, дифениламинсульфокислота, фенилантраниловая кислота, ферроин и др.
Рассмотрим примеры некоторых редокс-индикаторов.
Дифениламин.Это соединение является одним из первых редокс-индикаторов, описанных в литературе. Сначала индикатор необратимо окисляется до бесцветного дифенилбензидина, который обратимо окисляется до дифенилбензидина фиолетового:
Стандартный потенциал дифениламина Е 0 = 0,76 В при [H + ] = 1моль/л, интервал перехода рТ = 0,76 ± 0,03. Если Е ≤ 0,73 В, индикатор бесцветен, при Е ≥ 0,79 В имеет интенсивную сине-фиолетовую окраску.
В качестве окислительно-восстановительного индикатора используется также дифениламинсульфокислота. Её преимущество заключается в том, что в виде натриевой или бариевой соли она хорошо растворяется в воде. Механизм изменения окраски тот же, что и у дифениламина, но переход окраски наблюдается при потенциале 0,85 В – значительно выше, чем в случае использования дифениламина.
N-фенилантраниловая кислота. Реакция окисления аналогична реакциям, протекающим с другими дифениламинами:
Стандартный потенциал данного индикатораЕ 0 = 1,08 В.
У фенилантраниловой кислоты восстановленная форма бесцветная, окисленная – красно-фиолетовая рТ = 1,022 —1,138 В. Такой интервал изменения окраски соответствует скачку титрования раствора FeSO4 раствором KMnO4. Т.е. при добавлении данного индикатора к раствору FeSO4 он будет находиться в восстановленной бесцветной форме, а после достижения точки эквивалентности одна лишняя капля KMnO4 окислит индикатор и он перейдет в окисленную красно-фиолетовую форму. Данный индикатор применяется при определении содержания хрома методом перманганатометрии, т.к. образуется раствор, окрашенный в зеленый цвет и безиндикаторное титрование невозможно.
Ферроин. Этот индикатор представляет собой комплексное соединение железа (II) с 1,10-фенантролином. Комплекс окрашен в красный цвет:
При окислении ферроина образуется комплекс железа (III) бледно-голубого цвета: [Fe II (C12H8N2)3] 2+ 
Стандартный потенциал данного индикатораЕ 0 = 1,06 В в 1М серной или соляной кислотах. Потенциал ферроина можно в значительной степени изменить введением в ядро 1,10-фенантролина различных заместителей. При этом реальный потенциал можно варьировать от 0,84 до 1,10 В.