На что указывает выявление igg к пищевым продуктам в крови
Определение специфических IgG-антител к пищевым продуктам в диагностике пищевой аллергии: миф или реальность?
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В последнее время все большее количество врачей применяют в своей повседневной практике анализ, определяющий уровень 4-го субкласса специфических иммуноглобулинов G (IgG4) антител к пищевым продуктам с целью постановки диагноза пищевой аллергии. Активное применение этой методики подтолкнуло нас к написанию статьи на эту тему.
Поскольку очень многие пациенты ошибочно верят, что имеющие у них место аллергоподобные реакции вызваны именно пищевыми продуктами, и желают получить документальное подтверждение этой уверенности, тест на аллерген-специфические IgG4 представляет высокий коммерческий интерес для частных клиник. Эта дорогостоящая методика может приносить существенный доход, учитывая количество людей, обращающихся с жалобами на наличие пищевой аллергии. Распространенным подходом является определение уровня специфических IgG4 в сыворотке крови к широкому спектру продуктов при помощи иммуноферментного анализа или радиоаллергосорбентного теста – эта методика нашла применение не только в педиатрической практике, но и у взрослых.
Несмотря на то что очень часто в образцах обнаруживаются высокие уровни аллерген-специфических IgG4, они крайне редко сочетаются с релевантными клиническими проявлениями. Присутствие аллерген-специфических IgG4 ни в коем случае не говорит о наличии гиперчувствительности, а является физиологическим ответом на систематический контакт с пищевым продуктом.
На сегодняшний день отсутствует убедительная доказательная база, подтверждающая клиническую ценность данной методики в диагностике пищевой аллергии у детей. Нет никаких оснований предполагать, что аллерген-специфические IgG4 принимают активное участие в регулировании механизмов, связанных с пищевой непереносимостью. Таким образом, данная методика не рекомендована к применению в диагностике как пищевой аллергии, так и пищевой непереносимости, что соответствует целому ряду рекомендательных документов, которые легли в основу этой статьи.
Ключевые слова: аллергия, аллергические заболевания, пищевая аллергия, IgG4.
Для цитирования: Мунблит Д.Б., Корсунский И.А. Определение специфических IgG-антител к пищевым продуктам в диагностике пищевой аллергии: миф или реальность? // РМЖ. 2016. № 18. С. 1206–1209.
Для цитирования: Мунблит Д.Б., Корсунский И.А. Определение специфических IgG-антител к пищевым продуктам в диагностике пищевой аллергии: миф или реальность? РМЖ. 2016;18:1206-1209.
Detection of specific IgG against foods in food allergy diagnosis: myth or reality?
MD, MSc, PhD Munblit D.B. 1,3 Korsunskiy I.A. 2,3
1 Imperial College London, London, UK
2 Children’s City Hospital №9, Moscow, Russia
3 Faculty of Pediatrics, I. M. Sechenov First Moscow State Medical University, Moscow, Russia
In the recent years ammount of physicians using serological tests for immunoglobulin G4 (IgG4) in food allergy diagnosis is on the rise. Many patients believe that their symptoms are caused by food allergy which makes IgG4 testing commercially attractive for private practice. This expensive test may generate substantial income, considering the number of patients reporting “food allergy”. The most common approach is blood serum IgG4 measurement to a wide range of foods and it is used both, in paediatric and adult practice. Active use of this method in clinical practice is the main reason behind this paper write-up.
Despite detection of high levels of IgG4 they show clinical relevance in extremely rare circumstances. IgG4 presence is a normal physiological response to a systematic contact with a particular food product but does not represent a sign of atopy/allergy.
At present, there is no evidence base in support of this method use in food allergy diagnosis. There is also no data to consider IgG4 active involvement in mechanisms related to food intolerance. Therefore, this method is not recommended for use in diagnosis of food allergy and/or intolerance, as summarised in a number of consensus papers which makes a basis for this manuscript.
Key words: аllergy, allergic diseases, food allergy, IgG4.
For citation: Munblit D.B., Korsunskiy I.A. Detection of specific IgG against foods in food allergy diagnosis: myth or reality? // RMJ. 2016. № 18. P. 1206–1209.
Статья посвящена вопросу определения специфических IgG-антител к пищевым продуктам в диагностике пищевой аллергии
Распространенность аллергических заболеваний составляет около 10% в общей популяции и около 20–30% детей группы риска по развитию аллергии. Пищевая аллергия является одним из самых распространенных аллергических заболеваний в развитых странах и встречается у 2–3% взрослого и 6–8% детского населения Европы и США [1]. К наиболее часто встречающимся аллергенам относятся коровье молоко, яйца, арахис, орехи, пшеница, а также рыба и морепродукты [2]. Спектр симптомов пищевой аллергии может варьироваться от легких кожных проявлений до тяжелых, жизнеугрожающих анафилактических реакций.
Восприятие и понимание обществом термина «пищевая аллергия» очень отличается от его трактовки профессионалами, и более чем 20% людей связывают имеющие у них место аллергоподобные реакции с употреблением в пищу конкретных продуктов, зачастую ошибочно называя себя аллергиками. Диагностика пищевой аллергии начинается с детального сбора анамнеза и внимательного осмотра пациента, после чего специалист переходит к применению различных методов обследования in vivo и in vitro. Целью данной статьи не является подробное рассмотрение классических, повсеместно рекомендованных диагностических методов: кожных проб, измерения уровня специфических иммуноглобулинов E (sIgE) к различным пищевым продуктам или провокационных проб. Основным объектом обсуждения будет метод, который активно применяется в альтернативной медицине, а теперь все чаще и в традиционной – измерения уровня 4-го субкласса специфических иммуноглобулинов G (IgG), или IgG4-антител к пищевым продуктам.
Пищевая аллергия и непереносимость
Атипичная реакция на употребление в пищу конкретного продукта может быть проявлением пищевой аллергии или непереносимости.
Пищевая аллергия – это иммунологическая реакция, в основе которой лежит IgE-механизм. Она обычно проявляется непосредственно после употребления в пищу продукта, развивается быстро, и ее классическим примером может служить анафилаксия [3].
Пищевую аллергию не всегда просто диагностировать, и ее часто путают с пищевой непереносимостью. Термин «пищевая непереносимость» обычно используют для обозначения неиммунологической реакции организма, которая может развиваться в качестве ответа на употребление в пищу продукта или пищевой добавки [3].
Целью постановки диагноза «пищевая аллергия» является установление связи между клиничеcкими симптомами, которые отмечает пациент при употреблении в пищу конкретного пищевого продукта, и иммунологическим характером реакции. Установление причинно-значимого аллергена и механизма, лежащего в основе симптоматики, чрезвычайно важно, т. к. помогает избежать ненужных диет, которые могут нанести вред здоровью пациента.
Стандартные методы диагностики пищевой аллергии
Согласно существующим на сегодняшний день рекомендациям, сбор анамнеза, осмотр пациента, элиминационные диеты, кожные пробы или измерение уровня sIgE-антител, а также провокационные пробы с причинно-значимым продуктом являются рутинными методами, которые должны применяться для диагностики пищевой аллергии [4]. Еще одним методом, в поддержку которого говорят данные последних исследований, является «новое поколение» анализа sIgE – так называемая компонентная диагностика, которая позволяет определять уровни sIgE к молекулам аллергенов или специфических белков, из которых состоит тот или иной продукт [5].
На протяжении многих десятилетий для выявления наличия сенсибилизации к аллергену использовались кожные пробы. Из множества техник выполнения кожных проб наибольшую простоту применения и воспроизводимость результатов показали прик-тесты. Помимо чрезвычайной простоты метода, необходимо отметить и его дешевизну в сравнении с лабораторными исследованиями. Для его проведения могут использоваться как растворы аллергенов фабричного производства, так и натуральные продукты, применение которых зачастую несет более высокую диагностическую ценность [6]. Еще одним несомненным преимуществом метода является возможность прогнозирования вероятности пищевой аллергии в зависимости от величины положительной реакции. Так, например, Hill et al. показали, что вероятность наличия пищевой аллергии к коровьему молоку приближается к 100% при диаметре папулы 8 мм и больше, к куриному яйцу – 7 мм и к арахису – 8 мм [7], что подтверждается результатами проведенных провокационных проб.
Измерение уровня sIgE к пищевым продуктам в сыворотке крови играет важную роль в диагностике пищевой аллергии. Технологический прогресс позволил измерять аллерген-специфические IgE-антитела как в сыворотке крови, так и на поверхности базофилов. Применение данного метода может быть полезным не только с диагностической точки зрения, но и при планировании иммунотерапии, а также для прогнозирования последующего течения аллергического заболевания [5]. Так, более высокие уровни sIgE могут говорить о худшем прогнозе, в сравнении с низкими значениями, а снижение уровня sIgE к конкретному аллергену с течением времени может говорить о разрешении аллергии [8].
Положительные результаты, полученные при применении вышеупомянутых диагностических методик, говорят о сенсибилизации к конкретному аллергену, но сами по себе не являются подтверждением диагноза «пищевая аллергия». Диагноз ставится на основе комбинации данных клинического анамнеза и наличия положительной кожной пробы или выявленных sIgE к конкретному пищевому продукту. Единственным же методом, который позволяет практически гарантированно убедиться в наличии пищевой аллергии у конкретного пациента, является провокационная проба с причинно-значимым аллергеном [9].
Провокационная проба с пищевым продуктом считается «золотым стандартом» диагностики пищевой аллергии и единственным методом, который позволяет с уверенностью сказать, является ли конкретный пищевой продукт причиной клинических проявлений [10]. Данный метод используется как с целью постановки диагноза «пищевая аллергия», так и для подтверждения разрешения пищевой аллергии [9].
В ситуациях, когда врач, используя общепринятые методы диагностики, не может подтвердить наличие диагноза «пищевая аллергия», пациенты зачастую не могут смириться с данным фактом, продолжая во всем винить пищевые продукты. В этой непростой ситуации они, стремясь найти подтверждение своим теориям, используют те исследования, результаты которых отвечают их ожиданиям [11]. Зачастую таким исследованием становится анализ на определение аллерген-специфических IgG к пищевым продуктам.
Определение аллерген-специфических IgG4 к пищевым продуктам
В основе данного метода лежит забор крови и ее последующий анализ in vitro при помощи разновидностей иммуноферментного анализа [12]. Проводится оценка степени связывания IgG либо субкласса IgG4 с конкретным пищевым продуктом.
Анализ на sIgG зачастую представляет собой длинный список различных продуктов, распределенных на группы. Так, например, в категории молочных продуктов могут встречаться сыр чеддер, сыр эдам, йогурт, коровье молоко и т. д. Данный подход полностью противоречит существующим на сегодняшний день знаниям о природе пищевой аллергии. Аллергическая реакция развивается не на сорт сыра или йогурта, а на конкретный белок, который входит в состав молока и молочных продуктов (казеин, β–лактоглобулин и т. д.) [13]. Также в списке тестируемых продуктов часто обнаруживаются встречающиеся повсеместно ингредиенты, например сахар или дрожжи, которые чрезвычайно сложно полностью исключить из диеты и которые никогда не относились к числу распространенных аллергенов.
Уровни IgG-антител к пищевым продуктам в норме определяются в сыворотке крови здоровых людей (как взрослых, так и детей) без какой-либо видимой связи с аллергическими заболеваниями [14]. Более того, было показано, что повышенные уровни sIgG4 к пищевым продуктам у детей грудного возраста совместимы с толерантностью к этим продуктам в более старшем возрасте [15]. Взаимосвязь IgG4 и пищи также изучалась в рамках исследований по проведению оральной иммунотерапии. Попытки формирования толерантности к таким аллергенам, как арахис или коровье молоко, сопровождались повышением уровня sIgG к этим продуктам [16]. Также известно, что благодаря активности T-регуляторных клеток аллерген-специфические IgG4 образуются в процессе прохождения пациентом аллерген-специфической иммунотерапии и ассоциированы с формированием толерантности в результате долгосрочного воздействия аллергена [17]. Таким образом, можно считать IgG4 маркером экспозиции к аллергену и, возможно, маркером развития толерантности.
Несмотря на вышесказанное, некоторые врачи полагают, что sIgG могут быть причиной аллергической реакции немедленного или замедленного типа, пищевой непереносимости или других необычных ответов организма на прием пищи, хотя качественной доказательной базы под данными заявлениями нет [12]. Как в России, так и в европейских странах, многочисленные коммерческие лаборатории предлагают услугу исследования сыворотки крови на sIgG4 к широкому спектру пищевых продуктов, говоря о том, что данный метод является надежным способом диагностики пищевой аллергии.
По всей видимости, данная уверенность базируется на сведениях более чем тридцатилетней давности о том, что IgG4 может приводить к выбросу гистамина из базофилов, наподобие того, как это делает IgE [18]. С тех давних пор способность IgG4-антител приводить к выбросу гистамина из базофилов остается предметом дискуссий, однако убедительных доказательств этого факта так и не было получено [5]. За все время изучения этого вопроса авторы всего одного исследования смогли показать участие аллерген-специфического IgG4 в выбросе гистамина, используя экспериментальную модель [19]. Интересно, что в подобной модели сходный эффект показал и IgG1. Авторы последующих работ пришли к выводу, что на самом деле в этот механизм вовлечен IgE-рецептор, который перекрестно связывается через комплекс рецептора, находящегося на мембране базофила [20]. Эти наблюдения хорошо сочетаются с данными клинических наблюдений, которые показывают, что уровни IgG или IgG4 не коррелируют с подтвержденной пищевой аллергией (согласно данным провокационных проб) [21]. Также было выявлено, что высокие уровни sIgG4 к пищевым продуктам не связаны с клиническими проявлениями атопического дерматита [22].
Возникает закономерный вопрос, есть ли место анализу на sIgG у пациентов, страдающих аллергией, и какова диагностическая ценность данного метода? Примером использования IgG является тестирование на преципитирующие антитела, которые вовлечены в аллергические реакции III типа, как, например, при аллергическом альвеолите.
Применение теста на sIgG к пищевым продуктам оправдано в очень редких ситуациях, таких как определение IgG-антител к глиадину для диагностики целиакии, однако чувствительность и специфичность данного метода не очень высока и он должен использоваться исключительно в случае дефицита IgA [11].
Использование же данной методики с целью диагностики пищевой аллергии или непереносимости, как показывают результаты лабораторных экспериментов и клинических исследований, абсолютно неоправданно [11].
Международные согласительные документы
Применение метода определения аллерген-специфических IgG4 стало настолько широко использоваться коммерческими клиниками и активно применяться врачами, несмотря на отсутствие качественной доказательной базы, что этот факт вызвал крайнюю озабоченность аллергологического сообщества по всему миру. В 2008 г. Европейская академия аллергологии и клинической иммунологии (EAACI) опубликовала согласительный документ [11], в котором категорически не рекомендовала использование данной методики для диагностики как пищевой аллергии, так и непереносимости по причине отсутствия качественной доказательной базы. В поддержку этого документа выступили Американская академия аллергологии астмы и иммунологии (AAAAI) [23] и Канадское общество аллергологии и клинической иммунологии (CSACI) [24], полностью соглашаясь с мнением европейских коллег.
Согласительный документ по диагностике и лечению пищевой аллергии относит анализ определения аллерген-специфических IgG к нестандартизованным методикам и ставит его в один ряд с анализом волос или электродермальным (VEGA) тестированием [4].
Выводы
Подводя итог вышесказанному, мы приводим перечень основных выводов, касающихся применения метода определения аллерген-специфических IgG и базирующихся на мнении экспертов AAAAI [23].
1. На сегодняшний день не представляется возможным поставить диагноз «пищевая аллергия», основываясь лишь на определении антител к пищевому продукту в сыворотке крови, при отсутствии четкого клинического анамнеза или положительного результата провокационной пробы.
2. Наличие в сыворотке крови sIgG/sIgG4 или sIgE показывает наличие данных антител, но их присутствие не является достаточным для постановки диагноза. Само по себе наличие антител не говорит о том, что пациент страдает от пищевой аллергии.
3. Некоторые специалисты любят назначать тест на sIgG/IgG4 к пищевым продуктам и при их обнаружении предписывают пациенту диеты, которые сильно ограничивают рацион и не являются адекватными с точки зрения нутрициологии и отрицательно влияют на качество жизни. Подобный подход категорически неприемлем.
4. Коммерческие лаборатории очень часто проводят активный маркетинг анализа на sIgG/sIgG4, рекламируя его во врачебной среде и представляя не совсем адекватную оценку его диагностической ценности. Мы настоятельно рекомендуем опираться на данные доказательной медицины и согласительные документы, а не на рекламные проспекты коммерческих клиник и компаний.
Суммируя все вышесказанное, подчеркнем, что определение аллерген-специфических IgG к пищевым продуктам в сыворотке крови не является необходимым анализом в диагностике пищевой аллергии или непереносимости. Наличие sIgG представляет собой нормальный физиологический ответ организма на контакт с пищей и не свидетельствует о наличии пищевой аллергии и/или непереносимости. Помимо этого, данный анализ приводит к дополнительной, неоправданной финансовой нагрузке, поскольку данное исследование не входит ни в иностранные, ни в российские стандарты оказания медицинской помощи и пациент вынужден оплачивать проведение этого анализа самостоятельно. Присоединяясь к экспертному мнению наших зарубежных коллег, мы настоятельно рекомендуем отказаться от применения данного анализа в диагностике пищевой аллергии и пищевой непереносимости.
Научное расследование. Что показывает ИФА на специфические IgG к пищевым антигенам?
Используемая терминология.
Антиген (англ. antigen от antibody-generator — «производитель антител») — любое вещество, которое организм рассматривает как чужеродное или потенциально опасное и против которого организм обычно начинает вырабатывать собственные антитела (иммунный ответ). Антитела (иммуноглобулины, ИГ, Ig) — белковые соединения плазмы крови, образующиеся в ответ на введение в организм человека бактерий, вирусов, белковых токсинов и других антигенов. Связываясь с активными участками (центрами) бактерий, грибов или вирусов, антитела нейтрализуют выделяемые ими токсические вещества, препятствуют размножению, обеспечивают их разрушение в реакциях фагоцитоза. Гиперчувствительность (hypersensitivity) – повышенная чувствительность организма к определенным веществам — антигенам. Опосредуется специфическими рецепторами или антителами, находящимися в свободном состоянии или связанными с мембранами клеток, участвующих в иммунной защите или иммунном ответе. Может определенное время иметь латентное присутствие и не проявляться клиническими реакциями. Гиперчувствительность связана с количественными характеристиками антигенов, такими как доза (дозозависимость). Чаще гиперчувствительность является основой развития патологических (аномальных) реакций иммунной системы (ИС) на различные антигены. В таком случае гиперчувствительность – это состояние организма, при котором защитные механизмы иммунной системы, направленные на охрану постоянства внутренней среды организма, не справляются с выводом продуктов метаболитов патологических иммунных реакций из организма в условиях включения всех выделительных систем ( почки, легкие, ЖКТ, слюнные железы, кожа).
Гиперчувствительность Тип I — анафилактический тип или немедленный. В иммунном ответе на антиген синтезируются иммуноглобулины класса Е(IgE), они циркулируют в свободном состоянии и далее фиксируются на Fc-рецепторах, расположенных на базофилах, эозинофилах, тучных клетках. Повторные попадания антигена, вызывает его связывание с фиксированными антителами IgE и ответную дегрануляцию клеток с выбросом медиаторов воспаления, прежде всего гистамина.
Пищевая аллергия (food allergy) – проявляется в виде воспалительных реакций по механизмам «гиперчувствительности I типа» иммунной системы на белки или компоненты пищи, опосредованные иммуноглобулинами класса Е (IgE). Гиперчувствительность тип III – иммунокомплексный тип воспалительных реакций. Характеризуется образованием комплексов в составе антиген + специфическое антитело + компонент комплемента в состоянии циркуляции. Антителами выступают специфические иммуноглобулины классов G (IgG), М (IgM), A(IgA). Образующиеся циркулирующие иммунные комплексы должны быть элиминированы из организма с главной целью — выведение антигена. При хронической нагрузке антигенами и при активном их образовании, циркулирующие иммунные комплексы способны фиксироваться на рецепторах эндотелия мелких сосудов и клетках систем элиминации выделительных систем и вызывать воспалительные реакции к разрушенным аутоантигенам (собственным белкам) и структурам организма. Пищевая непереносимость (food intolerance): 1). Патологические реакции, возникающие на пищу или ее ингредиенты в результате генетических факторов и/или нарушения физиологических этапов пищеварения, которые запускают вторичные воспалительные реакции с участием иммунной системы. Вторичные воспалительные реакции (ВВР) развиваются по причинам контроля иммунной системой всех уровней пищеварения с целью обеспечения толерантности к пищевым антигенам. Процессы изменения антигенных характеристик пищевых продуктов нарушают их распознавание ИС на уровне иммунокомпетентных клеток. ВВР сопровождаются изменением соотношения про- и противовоспалительных цитокинов, перестройками регуляторных механизмов, направленных на обеспечение защитных реакций выведения причинных антигенов и восстановление гомеостаза организма. 2). Коммерческий термин, обозначающий суммарный комплекс патологических реакций на пищу, не принимающий во внимание закономерности системного иммунного воспаления. В связи с этим были введены и широко используются различные «тесты на пищевую непереносимость», характерные для определенной фазы взаимодействия пАГ с ИС. Иммуноферментный анализ (ИФА): (англ. Enzyme-Linked Immunosorbent Assay — ELISA) — лабораторный иммунологический метод, в основе которого лежит специфическая реакция «антиген-антитело», а определение образующегося комплекса производится благодаря ферментативной реакции окисления красителя. Чувствительность медицинского теста S1- отражает долю положительных результатов, которые правильно идентифицированы как таковые (иными словами чувствительность диагностического теста показывает вероятность того, что больной субъект будет классифицирован именно как больной), S1 = число больных, классифицируемые как больные/ общее число тестируемых больных.
Специфичность медицинского теста S2 — отражает долю отрицательных результатов, которые правильно идентифицированы как таковые (т.е. вероятность того, что не больные субъекты будут классифицированы именно как не больные), S2 = число здоровых, классифицируемые как здоровые/ общее число здоровых.
Чувствительность метода измерения — характеристика метода в виде наименьшего значения изменения физической величины, начиная с которого может осуществляться её измерение данным средством. Под чувствительностью ИФА понимается та минимальная концентрация определяемого реагента, при которой заметно различие в величине сигнала этой концентрации и образца, заведомо не содержащего определяемого реагента (отрицательный контроль). Эта разница в величине сигналов должна составлять 2 — 3 величины стандартного отклонения (СО) для отрицательного контроля.
Специфичность метода измерения подразумевает безошибочность диагностики именно требуемой физической величины или параметра: если результат ИФА положительный, значит, найдены именно те антитела или антигены, которые предполагались, а не какие-то другие.
Иммунодиетология™ — 1) термин, введенный авторами для обозначения нового направления иммунологии, изучающего различные этапы взаимодействия пищевых антигенов с иммунной системой; 2) зарегистрированный товарный знак (ТМ) компании ООО «Иммунохелс Рус».
Введение.
В конце 20-го века была выдвинута гипотеза, согласно которой при попадании пищи в желудочно-кишечный тракт, пищевые антигены (пАГ) проникают через кишечные стенки (интестинальный барьер) в кровеносную систему и, в ряде случаев, вызывают патологические реакции иммунной системы, которые в свою очередь, могут приводить к состоянию, известному в иммунологии, как состояние «гиперчувствительности» определенного типа. А состояние «гиперчувствительности», когда иммунная система не справляется с выведением из организма продуктов иммунных реакций, с большой вероятностью приводит к хроническим неинфекционным заболеваниям, часто именуемым «болезнями цивилизации». Основополагающая статья на эту тему появилась в России в 2000 г. (Розенталь В.М., Воейков В.Л., Волков А.В., Кондаков С.Э., Новиков К.Н. «Роль подбора индивидуального питания в экологической реабилитации человека». Материалы III-й международной конференции. Москва, МГУ, 24-25 ноября 2000. М.: Изд-во РАМН, 2000. с.243-247).
На протяжении последующих 20 лет учеными разных стран были разработаны тесты, позволяющие в лабораторных условиях «in vitro» регистрировать эффекты взаимодействия пАГ с иммунной системой человека, используя различные маркеры (измеряемые физические параметры) характерные для определенной фазы или типа взаимодействия пАГ с иммунной системой. Наиболее известные в США и Европе: York, ALCAT, NuTron, Cito, Prime, MRT, в России: Гемокод, РОЭ. Сравнительный анализ тестов приведен в работе (Розенштейн М.Ю., Розенштейн А.З., Кондаков С.Э., Черевко Н.А. «Современные лабораторные методы диагностики пищевой непереносимости». Бюллетень сибирской медицины, 2016, том 15, № 16, с. 69–78.).
Наиболее распространенным в клинической практике является York тест, разработанный York Nutrition Laboratories (UK) в 90-х годах прошлого века, или ИФА на специфические иммуноглобулины класса G (IgG) — в английской транскрипции ELISA IgG. Маркером в данном тесте является концентрация сывороточных специфических IgG к конкретному пАГ, измеряемая методом иммуноферментного анализа (ИФА). Впоследствии, многие известные лаборатории мира, вывели на рынок аналогичный тест, но уже под своим именем: Biomerica, Us Biotek, Genova Diagnostic, Meta Metrics, White Plane, Everly Well, Pinner test (США), ImmuPro, Dr. Fooke, R-Biopharm (Германия); Инвитро, Иммунохелс, Вектор Бест, Иммунотек, G-тест, Иммуновет (РФ). Что именно предлагается на рынках можно представить по характеру рекламы: IgG Food Intolerance Test (IgG тест на пищевую непереносимость), IgG Food Allergy Test (IgG тест на пищевую аллергию), IgG Food Sensitivity Test (IgG тест на чувствительность к пище). Заметим, что речь идет об одном и том же тесте ИФА на IgG к пищевым антигенам. При одинаковом маркере, различие только в наборе пАГ на тест- системе и методе обработки данных.
2. Существует ли критерий для корректного построения элиминационных диет на основе данных теста ИФА на IgG к пАГ и чем отличается используемая нами «методика Immunohealth™» от всех остальных тестов?
Задача данного научного расследования — дать врачам и всем заинтересованным читателям физически корректный и грамотный ответ.
Физическая модель ИФА на специфические IgG к пАГ.
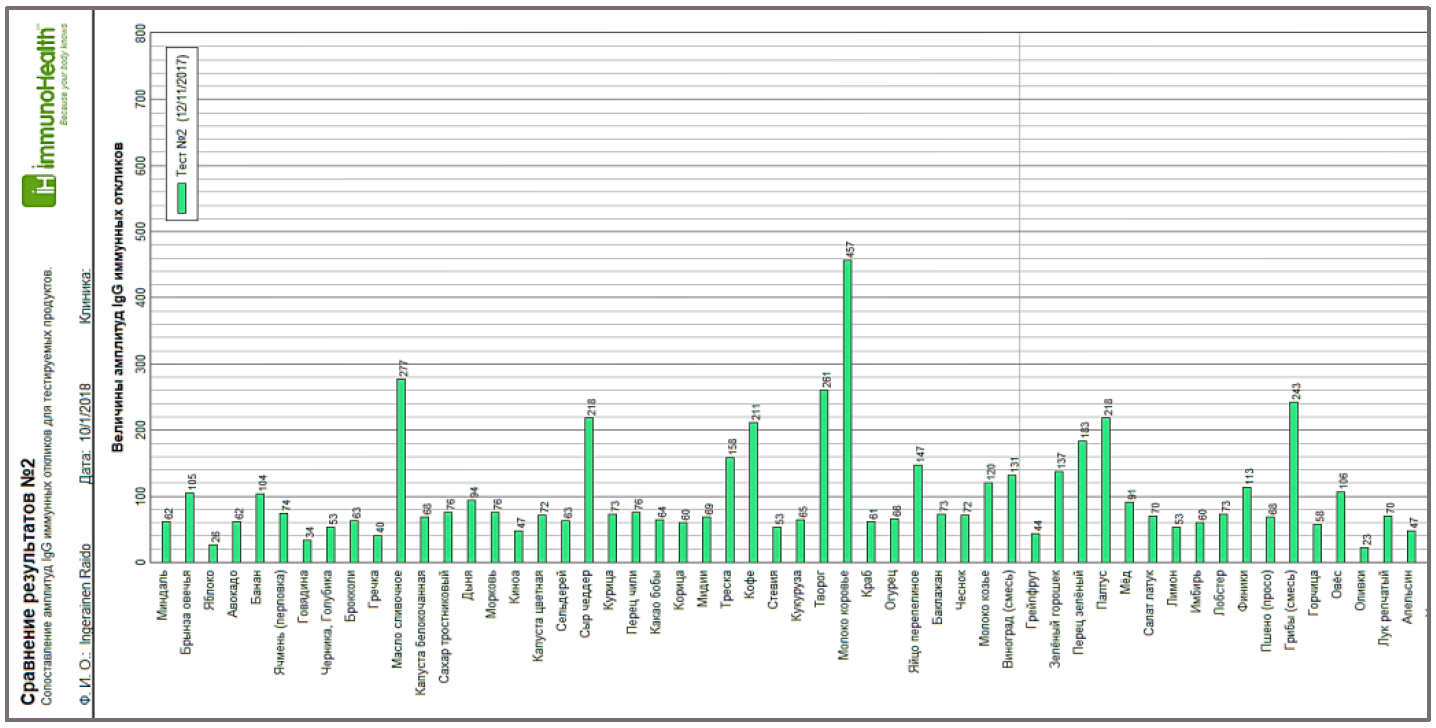
В тесте ИФА на IgG к антигенам из пищевых продуктов последние наносятся на лунки иммунологических плашек ячейки тест- системы для ИФА. В каждую ячейку добавляют равное количество сыворотки крови пациента. В результате взаимодействия специфических сывороточных антител иммунной системы (ИС) с каждым пАГ в образцах сыворотки крови получают порядка 100 иммунных откликов или 100 (для нашего случая) различных величин концентрации Сn(sIgG) специфических IgG. Таким образом, для решения задачи адаптации конкретного индивидуума к пищевой среде проводится эксперимент с его иммунной системой путем смешивания сыворотки крови со статистически представительной выборкой пАГ. Результат подобного тестирования представляет собой 100 значений величин концентраций Сn(sIgG), 1 ≤ n ≤ N, где N=100 — общее число тестируемых пАГ. Как правило, результат тестирования представляется графически в координатах «продукт — амплитуда маркера», Рис 1. Более того, в данной постановке эксперимента совершенно безразлично диагностируем ли мы здорового человека или больного аллергией или иным заболеванием. В том или другом случае, результаты теста ИФА на IgG к пАГ показывают как иммунная система каждого человека взаимодействует с тестируемым набором пищевых антигенов. Т.е. амплитуду IgG иммунных реакций ИС на каждый антиген, что и представлено на Рис 1. На этом лабораторный эксперимент по исследованию взаимодействия пАГ с ИС закончен.
Совершенно очевидно, что ИФА на IgG — диагностический тест, в ходе которого диагностируются процессы взаимодействия специфических иммуноглобулинов (sIgG) c представительной выборкой пАГ. Для описываемого метода ИФА на IgG к пАГ, как метода диагностики иммунных реакций «антиген-антитело» (пАГ-sIgG), характерны следующие оценки: — чувствительность 10−9 – 10−12 моль (вплоть до 10−21 моль в образце); — специфичность – порядка 100% (IgG); — относительная погрешность измерения единичного значения величины концентрации Сn(sIgG) мкг/мл — порядка 3.0-5.0%. Отметим, что медицинские определения «чувствительности S1» и «специфичности-S2», к тесту ИФА на IgG к пАГ, как методу диагностики иммунных реакций «антиген-антитело» (пАГ-sIgG), абсолютно неприменимы. Вывод: никакого отношения эксперимент ИФА на IgG к пАГ к диагностике «пищевой аллергии» не имеет и в этом отношении авторы солидарны с многочисленными критиками. Представьте себе мысленно физический эксперимент из школьного курса физики, аналогичный тому, что мы видим в случае ИФА на IgG к пАГ. Организм – «черный ящик» и мы по косвенным данным (однотипным откликам) должны что-то сказать о состоянии данного «ящика». Предположим, у Вас есть 100 одинаковых по размеру, но из различного материала шаров и Вы решили на расстоянии протестировать этими шарами стену дома, материал и форма которой Вам неизвестны (Рис 2).
Рис 2. Эксперимент по отражению шаров от объекта (стенки).
Вы бросаете перпендикулярно к стенке в локальную область один за другим все шары, они отскакивают от стены под разными углами и на разные расстояния, и на этом эксперимент по взаимодействию шаров со стенкой завершен. Дальнейшие ваши действия уже определяются задачей, поставленной вами перед началом эксперимента. Вас могут интересовать углы отскока, или распределение количества шаров по углам отражения, или длина отскока от стенки в зависимости от материала шаров и т.д. Эти задачи решаются методами, не имеющими отношения к самому эксперименту, только к набору данных по результатам эксперимента.
Вывод: Определение пищевой аллергии методом ИФА на IgG к пАГ является некорректно поставленной задачей тестирования.
Цель теста ИФА на IgG к пАГ.
C точки зрения прикладных задач диетологии, конечным результатом теста ИФА на IgG к пАГ, является не весь набор из 100 значений величин концентраций Сn (sIgG), найденных экспериментально (Рис 1), а только некоторая его часть, которая образована пАГ-антагонистами (пАГ–А), вызывающими патологические реакции ИС, потенциально приводящие к ситуации «гиперчувствительности Тип III» организма индивидуума. Таким образом: основной задачей и конечной целью тестирования реакций «пАГ- sIgG» на основе теста ИФА на IgG к пАГ является исключительно идентификация персонифицированных патологических иммунокомплексных реакций и соответствующих пАГ-А, инициирующих данные реакции. Именно на исключении из рациона пациента пАГ-А, найденных по результатам теста и основывается персонифицированная элиминационная диета: (Розенштейн М.Ю., Розенштейн А.З., Кондаков С.Э., Черевко Н.А. Новый методологический подход к созданию персонифицированной элиминационной диеты при пищевой непереносимости, обусловленной иммунопатологическими реакциями III типа. Бюллетень сибирской медицины, 2015, том 14, № 4, с. 60–67). Встает закономерный вопрос: а как идентифицировать именно патологические реакции по результатам многокомпонентного теста ИФА на IgG к пАГ? (многокомпонентность вызывается тем фактором, что мы проводим единичный ИФА на IgG в каждой n-й ячейке (1 ≤ n≤ N, где N — количество тестируемых пАГ) иммунологической панели. В дальнейшем мы будем использовать более краткую запись многокомпонентного теста ИФА на IgG к пАГ в виде (ELISA IgG)n.
В аллергологии вопрос идентификации патологических иммунных реакций, опосредованных иммуноглобулинами класса Е (IgE), приводящих к «гиперчувствительности Тип I» (аллергические реакции), решается путем экспериментального определения «референтных интервалов» и соответствующих критериев «норма — патология» (“cut-off” criterion), статистически достоверно связанных с наблюдаемой клинической картиной. При этом, основой идентификации реакций «гиперчувствительности Тип I» и инициирующих АГ по результатам теста ИФА на IgE (ELISA IgЕ)n, является только величина титра, или величина концентрации специфических иммуноглобулинов класса Е (IgE) к определенному аллергену (в том числе пАГ).
В отличие от аллергических реакций, опосредованных иммуноглобулинами класса Е (IgE), для иммунокомплексных реакций «пАГ-sIgG», корректное введение «референтных интервалов» и критериев «норма-патология» (в «аллергологическом смысле») принципиально невозможно, поскольку не известны значения концентраций специфических антител класса G к пАГ, при превышении которых наступает клиническая (патологическая) реакция на данный пАГ. Известны только «референтные интервалы» для концентраций общего IgG в крови (стандарт ВОЗ — WHO 67/69).
Несмотря на принципиальные отличия в биохимических свойствах иммуноглобулинов класса E и G, для идентификации патологических иммунокомплексных реакций «пАГ-sIgG», каждая лаборатория, по образу и подобию с анализом на иммуноглобулины класса Е, вводит свои собственные искусственные референтные интервалы, исходя из принятых значений калибраторов, определяющих диапазон величин титров IgG. Критерий «норма-патология», как правило, фиксируется на уровне половины диапазона измерений и является фиксированной величиной для всех тестов. Таким образом, протокол обработки данных теста ИФА на IgG к пАГ формально приводится в соответствие с протоколом, принятым в аллергологии для обработки результатов теста ИФА на IgЕ к пАГ. Именно этот подход использует большинство ведущих лабораторий мира: York-Nutrition, ImmuPro, Dr. Fooke, Biomerica, US Biotek, Genova Diagnostic, Meta Merix, Pinner и др. Аналогичный подход используется и в тестах ALCAT, NuTron, Сito.
С нашей точки зрения, подобный искусственный “аллергологический” подход является физически некорректным и приводит к существенным ошибкам в идентификации патологических иммунокомплексных реакций.
В разработанном нами подходе (методика Immunohealth™), идентификация патологических иммунокомплексных реакций «пАГ-sIgG» по результатам теста (ELISA IgG)n к пАГ, проводится на основе информации о структуре функции плотности распределения вероятности — ФПРВ (Probability Density Function), регистрируемых в эксперименте титров Сn(sIgG), в диапазоне шкалы измерений (Рис 3).
Рис 3. Вид ФРПВ для i-го теста (ELISA IgG)ni. Ti- критерий «норма-аномалия». Tf- условный критерий «норма-патология», принятый в лабораторной практике. Na- количество аномальных реакций, регистрируемых согласно критерию «норма-аномалия», Naf- количество аномальных реакций, регистрируемых согласно условному критерию «норма-патология».
В «методике Immunohealth™» величина персонифицированного критерия «норма — аномалия», c заданной точностью определяется программным путем на основе статистического анализа экспериментальных данных многокомпонентного теста (ELISA IgG)n к пАГ по разработанным алгоритмам программой Immunohealth™ IT. Базовым требованием нахождения корректного значения величины критерия «норма-аномалия», является наличие статистически представительного набора значений титров Сn(sIgG), т.е. необходимо и достаточно, чтобы величина объема выборки N тестируемых пАГ, приближенно удовлетворяла соотношению N ≥ 80.
Погрешность теста (ELISA IgG)n, как правило определяют величиной погрешности измерения амплитуды одного иммунного отклика (Рис 1), т.е. единичного значения концентрации специфических иммуноглобулинов — Сn(sIgG). В реальности, величина погрешности теста определяется не только и не столько погрешностью измерения одного иммунного отклика, а в основном, погрешностью определения числа идентифицируемых патологических иммунокомплексных реакций и соответствующих пАГ. А погрешность в определении числа пАГ-А всецело определяется значением величины титра, корректно разделяющего структуры А и В в ФРПВ (Рис 3). При фиксированном значении титра Tf, принятом в большинстве лабораторий мира на уровне половины значений шкалы измерения (Рис. 3), относительная погрешность в определении числа пАГ-А находится в пределах от 60% до 100%. Использование же персонифицированного критерия «норма — аномалия», определяемого по «методике Immunohealth™», гарантирует минимальную погрешность в определении количества пАГ-А и приводит к идентификации «кластеров» интолерантности ИС к пАГ, объединенных определенным антигенным «сродством». Таким образом, «методика Immunohealth™» позволяет не только диагностировать иммунокомплексные реакции у здоровых и больных людей, но и находить с минимальной погрешностью число пАГ-А, инициирующих патологические иммунокомплексные реакции.
Предлагаемый подход был проверен в течение более чем 15 лет на выборке более 30000 пациентов из разных популяций (США, ЕС, РФ) и на тест- системах для теста (ELISA IgG)n различных производителей. Врачи, использующие «методику Immunohealth™,» в своей практике, отмечают устойчивый положительный клинический эффект с контролем показателей системного воспаления (СОЭ, СРБ, ИЛ6, ИЛ1, ТНФ альфа и т.д.). Патогенетически этот эффект выражается в снижении нагрузки на эффекторные иммунные реакции, направленные на элиминацию причинных пищевых АГ, что достигается соблюдением персонифицированной элиминационной диеты, построенный с использованием предложенного критерия “норма – аномалия”.
Предложенная методика дает специалистам разных профилей инструмент, позволяющий использовать персонифицированную идентификацию и элиминацию причинных пАГ для лечения и профилактики неинфекционных хронических заболеваний. Это особо важно для пациентов с признаками системного воспаления, патогенеза многих неинфекционных заболеваний, таких как метаболический синдром, профилактика ожирения, современные интестинально–энтеропатические расстройства и аутовоспалительные синдромы. Одновременно методика позволяет определять статус ИС и степень пищевой адаптации по отношении к пищевым антигенам окружающей пищевой среды у здоровых людей.
Выводы научного исследования:
1. Корректно выполненный многокомпонентный иммуноферментный анализ (ELISA IgG)n, на специфические к пищевым антигенам иммуноглобулины класса G (IgG), предельно точно показывает концентрацию специфических антител, которая является отражением картины взаимодействия иммунной системы человека (здорового или больного) для каждого n –го пищевого антигена из представительной выборки из N тестируемых антигенов.
2. В «методике Immunohealth™» многокомпонентный иммуноферментный анализ (ELISA IgG)n на специфические к пищевым антигенам IgG, используется для создания индивидуальной адаптационной диеты на основе математически обоснованного критерия «норма – аномалия». Это область диетологии, а более конкретно — иммунодиетологии. Следовательно тест (ELISA IgG)n и «методика Immunohealth™» не имеют никакого отношения к диагностике «пищевой аллергии».
3. Результаты проведенных исследований позволяют сделать вывод о том, что новое направление ИММУНОДИЕТОЛОГИЯ™, базирующееся на корректно используемом многокомпонентном тесте (ELISA IgG)n к пАГ является перспективным направлением современной диетологии, в котором физически корректно учитываются индивидуальные реакции иммунной системы организма на представительную выборку пАГ.