на какую смесь перейти после альфаре
Что такое смесь на основе гидролизата белка и как правильно ввести ее в рацион ребенка?
Любой белок может восприниматься иммунной системой как антиген (аллерген). Для того, чтобы уменьшить аллергенность белка, при производстве детских лечебных смесей его обрабатывают специальными ферментами, которые расщепляют длинную молекулу белка на короткие «кусочки». При производстве частично гидролизованного белка, в продукте остаются довольно длинные фрагменты белковых молекул, и иммунная система «узнает» их. Поэтому смеси на основе частично гидролизованного молочного белка (смеси с аббревиатурой ГА) используются только для профилактики аллергии.
А вот для лечения уже имеющейся аллергии на белки коровьего молока такие смеси не подходят. Тут нужен более глубокий гидролиз, такой, чтобы в смеси не оставалось «узнаваемых» иммунной системой фрагментов белковой молекулы. Это дает возможность иммунной системе «забыть аллерген», провести «перезагрузку» и сформировать толерантность к молочному белку. Соответственно, глубокий гидролизат предназначен уже для лечения аллергии на молочные белки.
Смесь на основе гидролизата белка в любом случае содержит не только сам гидролизат, но и все другие компоненты детской смеси – жиры, углеводы, минеральные вещества и витамины, как и обычная смесь. Поэтому она является полноценным питанием для ребенка первого года жизни в тех случаях, когда грудного молока нет или недостаточно.
Лечебную смесь должен назначить врач. Но, чтобы правильно ввести в питание ребенка смеси на основе гидролизата белка, важно знать их особенности и следовать некоторым правилам.
Смеси-гидролизаты и соевые смеси в диетотерапии детей с аллергией к белкам коровьего молока: критерии выбора

Дебютом атопических заболеваний в детском возрасте чаще всего становится пищевая аллергия (на первом году жизни чаще это аллергия к белкам коровьего молока) и атопический дерматит (АтД) или атопическая экзема. АтД обычно протекает в виде кожных, а АБКМ в
The first manifestation of atopic diseases in infancy and early childhood is connected with cow’s milk protein allergy (CMPA) and atopic dermatitis (AtD). CMPA is usually characterized by skin manifestations, gastrointestinal symptoms or in a mixed form. Atopic eczema performs with skin manifestation. Breast feeding is the best strategy for allergy prevention. In necessity of bottle feeding hypoallergenic formulas belong to the products of first line. Partial and extensive hydrolysates are intended for prevention of atopy, and extensive ones for dietetic treatment of AtD. Amino acid formulas are purposed for most resistant and severe cases. Soya based formulas have some particular indications as well, but only in case of their tolerance.
Дебютом атопических заболеваний в детском возрасте чаще всего становится пищевая аллергия (ПА) и собственно атопическая экзема или атопический дерматит (АтД). Его распространенность достигает 10–30% [1]. АтД протекает в виде кожных манифестаций и в 30% случаев, как правило, при тяжелом течении, сочетается с пищевой аллергией, в том числе аллергией к белкам коровьего молока (АБКМ). В течение последних лет произошла значительная трансформация в понимании этиологии и патогенеза АтД. Учитывая многообразие клинических проявлений и факторов, способствующих развитию заболевания, дерматологи, аллергологи-иммунологи и педиатры продолжают по-разному трактовать критерии диагностики и подходы к лечению и профилактике [1]. Ранее считалось, что АтД является прежде всего аллергическим заболеванием, а в настоящее время он в большей степени рассматривается как заболевание с нарушением эпидермального барьера. Существует гипотеза дуального воздействия аллергенов, когда первичное проникновение аллергена, в том числе белков коровьего молока, происходит через нарушенный кожный барьер, инициируя аллергическое воспаление, а оральное проникновение аллергена, наоборот, индуцирует выработку толерантности [2].
ПА по-прежнему остается актуальной проблемой педиатрии, особенно у детей грудного и раннего возраста. Эта актуальность прежде всего обусловлена высокой распространенностью ПА в этих возрастных группах. Так, доказанная ПА встречается в экономически развитых странах у 6–8% детей раннего возраста. Аллергические реакции к белкам коровьего молока отмечаются у 2–6% младенцев, преобладают IgE-зависимые механизмы [3,4].
Из всех пищевых аллергенов, встречающихся у детей первого года жизни, наиболее значимы белки коровьего молока (БКМ), среди которых наиболее аллергенны β-лактоглобулин, α-лактальбумин, бычий сывороточный альбумин, γ-глобулин, а также α- и β-казеины [5]. С одной стороны, именно раннее (в первые месяцы жизни) употребление в пищу БКМ играет важнейшую роль в развитии аллергической реакции к ним и формировании атопического дерматита [6], с другой — есть данные, что раннее небольшое поступление цельномолочного белка в составе детских молочных смесей может оказывать эффект индукции оральной толерантности [7]. Первоочередной стратегией защиты от аллергии остается грудное вскармливание, как минимум до 4–6 месяцев. Исключительно грудное вскармливание само по себе, как и его продолжительность, не играет существенной роли в предотвращении, в частности, атопической экземы, но играет протективную роль в снижении хронизации экземы в возрасте до 6 лет [8].
Грудное молоко — уникальный продукт, который обладает всеми необходимыми для ребенка нутриентами, с одной стороны, и содержит большое количество иммунологических факторов, в том числе уменьшающих развитие пищевой сенсибилизации, — с другой. К ним относятся секреторный IgA, олигосахариды, нуклеотиды, макрофаги, цитокины, простагландины, лактоферрин, лизоцим и др. Кроме того, присутствие в грудном молоке небольшого количества чужеродных белков, проникающих из пищи матери, способствует формированию пищевой толерантности у ребенка.
Когда по каким-либо причинам грудное вскармливание невозможно, детей из семей с высоким риском развития атопических заболеваний необходимо переводить на смеси на основе гидролизованного белка. Гипоаллергенные смеси на основе частично гидролизованных белков молока, согласно действующим рекомендациям Европейской академии аллергологии и клинической иммунологии (European Academy of Allergy and Clinical Immunology, EAACI) 2014 г., могут использоваться у детей из группы высокого риска развития атопических заболеваний как минимум до 4 месяцев. Пролонгированное применение гидролизованных смесей для профилактики аллергии у детей без клинических проявлений не имеет преимущества, так как не доказана их существенная роль в профилактике аллергии [7].
Частичные гидролизаты призваны решить задачу первичной профилактики — сформировать пищевую толерантность без развития иммунологической сенсибилизации. Группа смесей ГА является достаточно гетерогенной, так как гидролизаты у разных производителей могут значительно отличаться по степени гидролиза, остаточной антигенности и профилю распределения пептидов (ММР или молекулярно-массовому распределению).
В целом для всех смесей ГА характерны несколько признаков:
В настоящее время для профилактики аллергии используют гидролизаты сывороточных белков. Это более физиологично для ребенка, так как в сывороточной фракции находится подавляющее большинство незаменимых для младенца аминокислот.
Однако глубокогидролизованные смеси, созданные изначально для лечения АтД, также оказывают профилактический эффект, который может быть даже более выражен. Так, исследование GINI показало значительное снижение риска развития АтД у детей до 15 лет с отягощенным семейным аллергоанамнезом не только в группе детей, которые с первого года жизни получали частичный сывороточный гидролизат, но и в группе пациентов, получавших высокогидролизованную смесь на основе казеина. Объяснялось это тем, что в составе данной формулы помимо олигопептидов с низкой молекулярной массой также присутствует фракция пептидов, отвечающая за развитие пищевой толерантности. Поэтому важный вывод исследования GINI заключается в том, что невозможно предсказать, каким будет эффект смеси — лечебным и/или профилактическим, основываясь только на информации о субстрате гидролиза (сывороточные белки или казеин) и степени гидролиза (частичный или высокий). Для понимания эффекта каждого конкретного гидролизата необходимо иметь информацию о его «пептидном профиле», то есть о распределении пептидов по молекулярной массе в гидролизной смеси [9].
В качестве примера можно рассмотреть продукт Peptigen® IF-3080. Peptigen® IF-3080 представляет собой глубокий гидролизат сывороточных белков. 99% пептидов в его составе имеют молекулярную массу менее 3,5 кДа, в результате чего антигенность снижена в 100 000 раз по сравнению с БКМ, т. е. такой гидролизат не вызывает сенсибилизацию. Исследования данного продукта с глубоким гидролизом белков, низкой остаточной антигенностью и небольшим количеством лактозы подтвердили, что данный продукт может использоваться и в качестве профилактики, и для диетотерапии АБКМ при ее легком течении, кожных проявлениях [10–12].
Peptigen® IF-3080 входит в состав смеси Nutrilak Premium® Гипоаллергенный, предназначенной для диетического профилактического питания детей из групп риска по развитию пищевой аллергии с первых дней жизни. Состав смеси обеспечивает нормальные показатели роста и развития детей первого года жизни. Особенно интересны следующие нутриенты в составе формулы:
Добавление в гипоаллергенные смеси L. rhamnosus LGG® и B. lactis (BB-12®) с целью профилактики развития аллергических заболеваний – интересное и перспективное направление современной педиатрии. В настоящее время в научной литературе существуют рекомендации по назначению пробиотиков беременным в последнем триместре и кормящим женщинам из семей с отягощенным аллергоанамнезом. Исследования показали, что назначение пробиотиков кормящим матерям увеличивает продукцию трансформирующего фактора роста β в грудном молоке. А это в свою очередь стимулирует синтез секреторного IgA в кишечнике ребенка, что в конечном итоге предотвращает развитие пищевой сенсибилизации [13, 14]. Проведенный также метаанализ 17 исследований показал, что пробиотики снижают риск развития пищевой аллергии у детей из семей с высокой вероятностью формирования атопических заболеваний на 23%. Пробиотики можно назначать пре- и постнатально.
Несомненно, вопрос профилактики АтД и других атопических заболеваний при помощи пробиотиков требует дальнейшего изучения. Большое количество вопросов остается открытыми: в каких дозах, какими курсами, пре- или постнатально, какой пробиотик является наиболее эффективным и многое другое. На все эти вопросы еще предстоит ответить.
Тем не менее чем больше способов профилактики атопических заболеваний будет в арсенале врачей, тем выше вероятность того, что эта цель будет достигнута.
Всегда ли идеально грудное молоко?
Грудное вскармливание является наиболее предпочтительным для всех детей. Однако у младенцев исключительно на грудном вскармливании изредка наблюдаются симптомы аллергии, по данным литературы, около 0,5% детей на ГВ может коснуться эта проблема. Это связывают с попаданием аллергенов из рациона матери в грудное молоко и возникновением аллергической реакции. В подобных случаях кормящей матери рекомендуется исключить молоко и содержащие цельномолочный белок продукты из своего рациона и постараться выяснить, есть ли другие продукты в ее питании, которые провоцируют аллергию у ребенка. Только если все это не дало результата, приходится прекращать грудное вскармливание. Например, Isolauri и соавт. [15] рекомендуют прекращать грудное вскармливание у детей с атопическим дерматитом лишь в тех случаях, когда замедляются процессы роста. Кормящие грудью матери детей-атопиков должны быть обследованы диетологом, чтобы оценить адекватность их диеты и при необходимости внести коррективы, особенно при выявленном дефиците кальция.
Смеси на основе глубокогидролизованных белков и аминокислотные смеси для диетотерапии
Продукт первого выбора для диетотерапии АБКМ — это глубокогидролизованные смеси, их адекватно переносит большинство пациентов (90%) с IgE-опосредованными и не-IgE-опосредованными вариантами АБКМ разной степени тяжести. При отсутствии эффекта или изначально тяжелых вариантах течения АБКМ рекомендованы аминокислотные смеси [16–18].
Роль и место соевых смесей при АБКМ у детей
В повседневной жизни, и не только при АБКМ, в ряде стран довольно широко применяются соевые смеси (СС). Смеси на основе изолята соевого белка в течение многих лет используются без назначения врача и без медицинского контроля, поэтому среди клиницистов существуют различные мнения об их полезности и эффективности.
В 2003 г. в ряде стран приняли рекомендацию не использовать без специальных медицинских показаний соевые смеси в питании детей ранее 6-месячного возраста. Причиной послужило высокое содержание фитоэстрогенов [19]. В результаты группа экспертов пришла к соглашению, что соевые смеси можно рекомендовать детям с АБКМ при условии их хорошей переносимости, если ребенок не переносит (из-за вкусовых проблем) глубокие гидролизаты или аминокислотные смеси. Помимо вкусовых преимуществ соевые смеси более дешевые, чем гидролизаты, что может иметь значение для бюджета семьи.
До появления лечебных смесей на основе гидролизатов белка именно соевые смеси были единственными продуктами для детей с АБКМ. Однако соевый белок также относится к распространенным аллергенам. В составе белков сои выделены конглицинин (имеющий молекулярный вес 180 кДа) и глицинин (МВ 320 кДа) как основные аллергены, а также ингибитор трипсина как минорный аллерген. Именно эти три белка способны вызвать аллергию на соевый белок. Большинство детей с IgE-опосредованной АБКМ хорошо переносят соевые смеси. Комитет по питанию Европейского общества детских гастроэнтерологов, гепатологов и нутрициологов (European Society for Paediatric Gastroenterology Hepatology and Nutrition, ESPGHAN) в 1999 г. высказал точку зрения, что СС не являются продуктами выбора при АБКМ. В 2000 г. Комитет по питанию Американской Академии педиатрии отметил, что дети с IgE-опосредованной формой АБКМ могут успешно получать соевые смеси и в качестве стартовой диетотерапии, и после диетотерапии с использованием смесей-гидролизатов в возрасте старше 6 мес [19].
Смеси на основе изолята соевого белка внесли весомую лепту в диетотерапию АБКМ в предшествовавшие десятилетия до появления смесей-гидролизатов. Несмотря на постепенное сокращение клинического использования СС, они находят применение в схеме диетотерапии у детей старше 6 месяцев при отсутствии гастро-интестинальных проявлений (благодаря меньшей стоимости) при условии предварительного проведения клинической пробы на их хорошую переносимость у данного пациента [20]. В тех семьях, где придерживаются принципов вегетарианства или других религиозно-этических соображений и не употребляют коровье молоко, соевые смеси служат хорошим выбором для питания детей раннего возраста.
Литература
* ФГБОУ ДПО РМАНПО Минздрава России, Москва
** ФГАУ НМИЦЗД Минздрава России, Москва
*** АО «ИНФАПРИМ», Москва
Смеси-гидролизаты и соевые смеси в диетотерапии детей с аллергией к белкам коровьего молока: критерии выбора/ С. Г. Грибакин, А. Г. Тимофеева, О. А. Боковская
Для цитирования: Лечащий врач № 4/2020; Номера страниц в выпуске: 28-31
Теги: дети, новорожденные, атопический дерматит, экзема
Использование продуктов на основе гидролизата молочного белка при пищевой аллергии у детей раннего возраста
Пищевые аллергены являются наиболее частыми этиологическими факторами в развитии атопии на первом году жизни. Одним из основных аллергенов, вызывающих развитие пищевой аллергии у детей грудного возраста, является белок коровьего молока (БКМ) [1]. Данный п
Пищевые аллергены являются наиболее частыми этиологическими факторами в развитии атопии на первом году жизни. Одним из основных аллергенов, вызывающих развитие пищевой аллергии у детей грудного возраста, является белок коровьего молока (БКМ) [1]. Данный продукт содержит более 20 антигенов, из которых наибольшими аллергенными свойствами обладают β-лактоглобулин, казеин, α-лактальбумин, бычий сывороточный альбумин. Ингредиенты коровьего молока (казеин, сывороточные белки) могут присутствовать во многих пищевых продуктах. Известно, что на первом году жизни аллергия к белкам коровьего молока встречается у 2–7% младенцев, находящихся на искусственном и 0,5–1,5% детей на естественном вскармливании. Среди больных атопическим дерматитом у 85–90% детей диагностируется аллергия к белкам коровьего молока. К другим распространенным клиническим проявлениям аллергии к БКМ относятся гастроинтестинальные нарушения, такие, как обильные срыгивания и рвота, колики, изменение характера стула — диарея или запоры. Реже встречается симптоматика со стороны органов дыхания — одышка, приступы удушья, апноэ.
Диагностика аллергии к БКМ основана на тщательном сборе аллергологического анамнеза и оценке всей клинической симптоматики. Для верификации диагноза в остром периоде заболевания проводится аллергологическое обследование — определение уровней специфических антител — IgE и IgG4 в сыворотке крови, реже — кожные пробы. Выявление тем или иным способом сенсибилизации к БКМ является показанием для полного исключения из питания ребенка продуктов, содержащих молочные протеины.
В случаях выявления пищевой аллергии у детей, находящихся на естественном вскармливании, учитывая уникальные свойства материнского молока, необходимо сохранить его в питании ребенка в максимальном объеме. Кормящей матери назначают гипоаллергенную диету, при этом степень пищевых ограничений и набор продуктов достаточно индивидуальны и зависят в первую очередь от тяжести клинических проявлений аллергии у младенца. При недостатке или отсутствии грудного молока в питании ребенка с аллергией к белку коровьего молока используются безмолочные лечебные смеси. Согласно современным рекомендациям, в период клинических проявлений аллергии (острый период атопического дерматита, желудочно-кишечные симптомы), безусловно, наиболее целесообразным является назначение смесей на основе высокогидролизованного молочного белка как продуктов, практически лишенных антигенных свойств [2, 3, 4, 5, 6]. Все продукты данной группы обогащены комплексом витаминов, макро- и микроэлементов и соответствуют требованиям ВОЗ по ингредиентному составу, биологической и пищевой ценности, влиянию на физическое и психомоторное развитие детей первого года жизни. Появление высокогидролизованных смесей значительно расширило возможности диетотерапии у детей раннего возраста с пищевой аллергией.
В зависимости от степени расщепления молочного белка выделяют смеси на основе его высокого (экстенсивного) или частичного (умеренного) гидролиза. Установлено, что чем ниже молекулярная масса пептидов гидролизата, тем ниже его иммуногенность и меньше риск развития аллергических реакций на данный продукт. Так, молекулярная масса нативного белка коровьего молока колеблется от 10 до 60 кDa. Молекулярный вес пептидов, ниже которого аллергенность белкового гидролизата становится минимальной, составляет 2,5–3 кDa. Однако и в составе данных продуктов возможно сохранение остаточных количеств белковых антигенов, способных вызвать аллергические реакции у больных с аллергией к белку коровьего молока. Аллергенные свойства частично гидролизованных белков снижены в 300–1000 раз по сравнению с БКМ.
По клиническому предназначению смеси на основе гидролизатов молочного белка можно подразделить на лечебные, лечебно-профилактические и профилактические. Включение смеси в ту или иную группу зависит от степени гидролиза белкового субстрата, а также от доказанной клинической эффективности продукта.
К лечебным относятся только специализированные смеси, созданные на основе высокогидролизованного молочного белка: «Альфаре», «Нутрилак пептиди СЦТ», «Нутрилон Пепти ТСЦ», «Прегестимил», «Нутрамиген», «Фрисопеп», «Фрисопеп АС» и др.
Такие гипоаллергенные смеси на основе частично гидролизованного молочного белка, как «НАН ГА 1», «НАН ГА 2», «Нутрилон ГА 1» и «Нутрилон ГА 2» должны применяться только для профилактики аллергических заболеваний у детей из групп высокого риска по развитию атопии, переводимых на смешанное и искусственное вскармливание.
Пептидный профиль ряда смесей, предназначенных для профилактики аллергии, — «Нутрилак ГА», «ХиПП ГА 1», «ХиПП ГА 2», «Хумана ГА 1» и «Хумана ГА 2» — свидетельствует о достаточно высокой степени гидролиза белкового субстрата, что позволяет говорить о возможности их использования не только в профилактических целях, но и для лечения легких форм аллергии к белкам коровьего молока, протекающих без участия IgE-опосредуемых механизмов.
Гипоаллергенные продукты на основе частично гидролизованного белка также могут применяться на втором этапе диетотерапии — этапе расширения рациона.
Кроме степени гидролиза белка, смеси отличаются по исходному субстрату, подвергаемому гидролизу: большинство продуктов создано на основе гидролиза сывороточных белков. Смеси «Прегестимил», «Нутрамиген», «Фрисопеп АС» — продукты на основе гидролизата казеина.
Имеются также определенные отличия в жировом и углеводном компонентах, по витаминному составу. Учет особенностей каждой смеси позволяет подобрать продукт в соответствии с индивидуальными особенностями клинической картины заболевания. В состав липидного компонента лечебных смесей «Альфаре», «Нутрилак пептиди СЦТ», «Нутрилон Пепти ТСЦ», «Прегестимил», предназначенных в первую очередь для детей с гастроинтестинальными проявлениями ПА и синдромом мальабсорбции, введены среднецепочечные триглицериды (до 50% общего количества липидов), которые легко всасываются в систему воротной вены, минуя лимфатические сосуды, не требуя эмульгирования и участия панкреатической липазы.
Необходимо также учитывать наличие или отсутствие лактозы в составе углеводного компонента смеси, поскольку аллергия к белку коровьего молока нередко сопровождается непереносимостью лактозы. В таких случаях целесообразно назначать смесь на основе высокогидролизованного белка, не содержащую лактозу [3].
Новым направлением детской нутрициологии является обогащение продуктов питания про- и пребиотиками. Среди гипоаллергенных продуктов следует отметить следующие смеси, обогащенные пребиотиками, — «Беби ГА», «Нутрилон ГА 1 и 2», «Нутрилон Комфорт 1 и 2», «Хумана ГА 2», а также единственный гипоаллергенный продукт, обогащенный бифидобактериями — «НАН ГА 2». Разработан и производится, но к настоящему времени не представлен на российском рынке продуктов детского питания «Нутрамиген LGG» — лечебный гидролизат с добавлением лактобактерий. Данные продукты наиболее показаны при наличии у детей дисбиотических отклонений в составе микрофлоры кишечника.
Несмотря на общепризнанную эффективность смесей на основе гидролизата молочного белка, поиск новых более гипоаллергенных субстратов для гидролиза продолжается. Так, появились первые сообщения о результатах исследования смеси, приготовленной на основе гидролизата белка риса. Исследование, проведенное в группе здоровых детей, показало хорошую усвояемость данной смеси. Был показан лечебный эффект данной смеси у детей с аллергией к БКМ [7, 8].
Еще одна группа продуктов, используемых в питании детей с аллергией к БКМ, это соевые смеси. В состав данных продуктов, помимо изолята соевого белка, входят растительные масла, декстрин-мальтоза, витаминно-минеральный комплекс в соответствии с физиологическими потребностями детей первого года жизни. Данные смеси содержат нативный белок и потенциально аллергенны [9, 10, 11], в связи с этим использование их у детей с пищевой аллергией в настоящее время ограничено. Следует избегать назначения соевых смесей детям младше 5–6 мес, в остром периоде заболевания, при наличии тяжелых, особенно гастроинтестинальных проявлений аллергии. Выполнение данных правил позволяет избежать развития сенсибилизации к соевому белку и появления аллергических реакций.
Алгоритм выбора лечебного продукта в зависимости от клинических проявлений аллергии и характера сенсибилизации представлен на рис. 1.
Сроки элиминации молочных смесей и продуктов из питания детей с пищевой аллергией индивидуальны. Минимальная длительность безмолочного питания у детей с аллергией к белкам коровьего молока составляет 4–6 мес, в отдельных случаях может продолжаться до одного года и более. Молочные продукты вводят в рационы детей, начиная со смесей на основе частично гидролизованного белка. Осуществляют это в период клинико-лабораторной ремиссии заболевания, постепенно, учитывая возможность развития повторных аллергических реакций.
Отметим, что в настоящее время нет окончательно сформированного общепринятого мнения в отношении возможности использования у детей с пищевой аллергией таких продуктов, как смеси на основе частично гидролизованного молочного белка, кисломолочных смесей, продуктов на основе козьего молока.
Кроме того, даже приведенный выше взвешенный диетологический подход — подбор продукта — заменителя грудного молока на основании всех имеющихся клинических данных и результатов специфической диагностики, с учетом индивидуальных особенностей больного позволяет выбрать лишь группу продуктов (лечебные, лечебно-профилактические, профилактические смеси), но не конкретный продукт детского питания. Вместе с тем клиническая практика показывает, что переносимость различных продуктов в пределах одной и той же группы у каждого конкретного ребенка может значительно отличаться. Различия индивидуальной переносимости продуктов в значительной мере связаны с разнообразием состава смесей, особенностей технологической обработки их белкового компонента, состава углеводных и жировых компонентов продукта, витаминного и минерального компонентов и других добавок.
С целью оптимизации диетотерапии и индивидуального подбора смеси для максимального снижения риска индивидуальной реакции непереносимости смесей нами был использован новый диагностический тест «Ифа-Лакттест» (далее «Лакттест»). Набор реагентов разработан в Медицинском научно-исследовательском центре «Медиан» (патент РФ 2006126792/15/029074/ от 24.07.06.). Он предназначен для полуколичественного определения в крови ребенка методом иммуноферментного анализа (ИФА) содержания антител классов IgG, IgG4 и IgЕ, иммунореактивных в отношении белково-пептидных антигенов, содержащихся в продуктах детского питания различных типов. Набор позволяет также определять концентрацию специфических антител к белковым компонентам грудного, коровьего и козьего молока, сои, овса, глютена пшеницы, а также к фракциям белка коровьего молока (бычий сывороточный альбумин, казеин, β-лактоглобулин) и яйца (овальбумин).
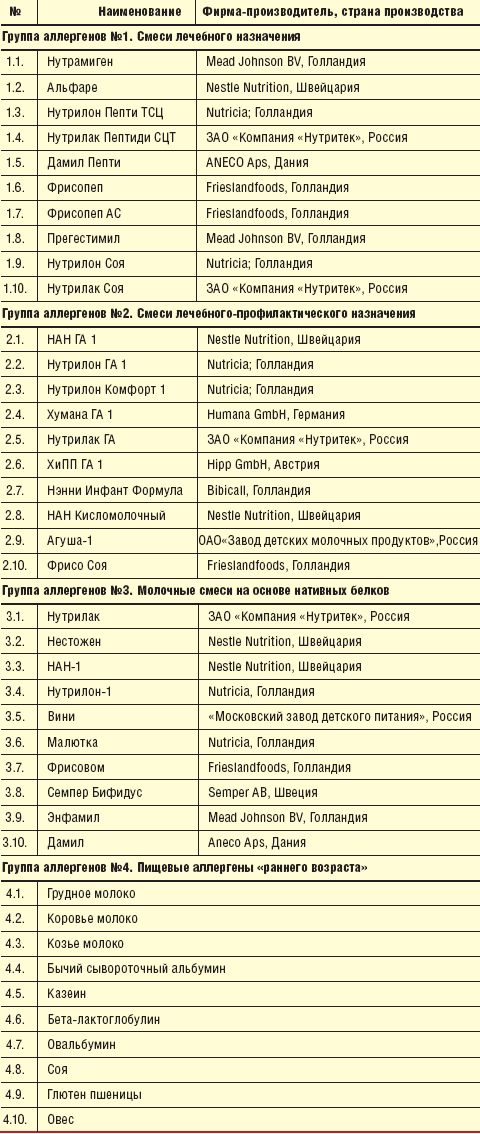
Используемые в наборе аллергены разделены на 4 группы (табл. 1), каждая из которых представлена на отдельном иммунологическом планшете (панели): 1-я группа включает суммарные белково-пептидные аллергены смесей лечебного назначения, 2-я — аллергены смесей профилактического назначения, 3-я — аллергены молочных смесей на основе нативных белков, 4-я — пищевые аллергены «раннего возраста». Данный набор аллергенов позволяет: во-первых, верифицировать диагноз аллергии к белку коровьего молока, поскольку включает аллерген белка коровьего молока и наиболее аллергенных его фракций (бычий сывороточный альбумин, β-лактоглобулин, казеин); во-вторых, наличие аллергена козьего молока позволяет выявить случаи перекрестной аллергии к козьему молоку; в-третьих, наличие в панели наиболее часто встречающихся пищевых аллергенов первого года жизни — сои, глютена, овальбумина — позволяет контролированно подбирать блюда прикорма; и наконец благодаря включению в состав панели грудного молока возможно оценить переносимость грудного молока детьми, находящимися на естественном вскармливании, и выявлять редко встречающиеся случаи непереносимости грудного молока. 1-я, 2-я и 3-я панели предназначены для индивидуального подбора специализированных смесей — заменителей грудного молока.
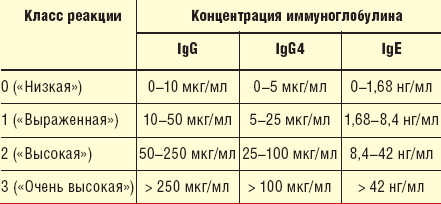
Содержание специфических антител оценивали полуколичественно в классах реакции. Каждый класс соответствует определенному диапазону концентраций иммуноглобулина (табл. 2).
У здоровых детей содержание специфических иммуноглобулинов характеризуется классом реакции 0. Повышение содержания антител к пищевым аллергенам (класс реакции 1 и выше) рассматривали как свидетельство сенсибилизации к данным аллергенам.
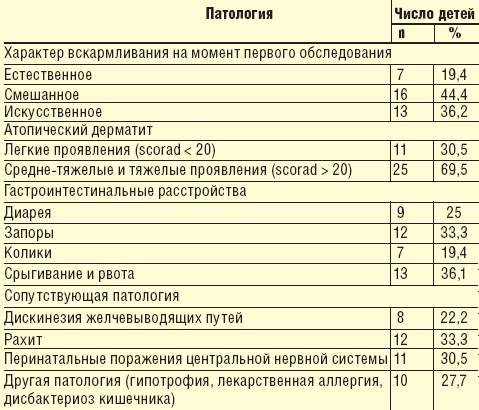
Оценка эффективности применения данного теста при назначении диетотерапии у детей с атопическим дерматитом первого года жизни нами была проведена у 36 детей, 58% из которых — мальчики, 15% — девочки в возрасте от 4 до 12 мес, находившихся на обследовании и лечении в Консультативно-диагностическом центре и отделении питания здорового и больного ребенка НЦЗД РАМН (табл. 3).
Длительность заболевания колебалась от 3 нед до 6 мес. Клиническое обследование детей проводилось по общепринятому плану и включало сбор анамнеза; оценку нутритивного статуса, клинических проявлений заболевания; инструментальные и лабораторные исследования (УЗИ органов брюшной полости, по показаниям — копрологическое исследование, определение экскреции углеводов с калом, исследование кишечной микрофлоры), аллергологическое обследование — определения методом ИФА специфических IgG4 к пищевым продуктам (анализ проводили в лаборатории клинической биохимии НЦЗД РАМН).
Выраженность проявлений атопического дерматита оценивали на момент обследования по индексу scorad. У 21 ребенка кожные проявления аллергии сопровождались симптоматикой со стороны желудочно-кишечного тракта, с помощью УЗИ в 8 случаях выявлены признаки дискинезии желчных путей, у 17 детей — реактивное увеличение поджелудочной железы.
Тщательный сбор аллергологического анамнеза позволил выявить четкие указания на аллергию к БКМ у 25 детей. Так, у 22 детей начало заболевания было связано с введением в питание детских смесей на основе нативных БКМ, в 9 случаях отмечалась отчетливая реакция в виде кожных высыпаний или гастроинтестинальной симптоматики при приеме продуктов, содержащих молочные протеины. У детей, находящихся на исключительно грудном вскармливании, во всех случаях имел место докорм молочной смесью в роддоме, употребление матерью значительного количества молочных продуктов во время кормления грудью.
Использование панели №4 (пищевые аллергены раннего возраста) благодаря возможности определять одновременно три класса антител — IgG, IgG4 и IgЕ позволило получить более полную информацию о характере пищевой сенсибилизации у каждого ребенка (табл. 4).
Благодаря комплексному обследованию с помощью «ЛАКТТЕСТ» сенсибилизация к БКМ была установлена у 86,1% обследованных детей, что превышает частоту выявления существующими методами. IgE опосредованная аллергия к БКМ диагностирована у 22 детей (55,9%), а IgE не опосредованная — у 9 (24,3%).
Сенсибилизация к белку козьего молока по данным «Лакттест» была выявлена у 24 детей (66,7%). При этом сенсибилизация к данному белку отмечалась у детей как получавших (7 детей), так и не получавших (17 детей) продукты на основе козьего молока. Сенсибилизация к козьему молоку всегда сочеталась с сенсибилизацией к БКМ, что указывает на наличие перекрестной аллергической реакции. Аллергия к белку сои выявлена у 3 детей, при этом 2 больных ранее не получали соевых смесей, аллергия к овальбумину — у 3 детей, к глютену пшеницы — у 2 детей.
У всех детей с сенсибилизацией к БКМ была обнаружена повышенная иммунореактивность иммуноглобулинов одного или нескольких классов в отношении всех смесей на основе нативных белков коровьего молока (панель №3), однако выраженность реакции с аллергенами разных смесей у каждого ребенка была неодинакова и варьировалась в пределах от 1 до 3 класса реакции.
Наиболее интересные результаты были получены при анализе данных панели №1 (смеси лечебного назначения) и панели №2 (смеси лечебно-профилактического и профилактического назначения). Данные об индивидуальной переносимости смесей сопоставлялись с характером выявленной сенсибилизации, полученным при использовании панели №4. В первую очередь следует отметить, что индивидуальная переносимость смесей значительно отличалась даже для, казалось бы, аналогичных продуктов. Непереносимость смесей на основе частично гидролизованного молочного белка «НАН ГА 1», «Нутрилон ГА 1», «Нутрилон Комфорт 1», «Хумана ГА 1», «Нутрилак ГА», «ХиПП ГА 1» отмечалась у детей с подтвержденной аллергией к БКМ и имела значительные индивидуальные различия. Выявление непереносимости той или иной смеси не зависело от того, получал ли ее ребенок до начала обследования.
Непереносимость смеси «Нэнни», произведенной на основе козьего молока установлена у 24 больных (обнаружение сенсибилизации к белку козьего молока). Однако у 2 детей с выявленным диагностически значимым уровнем IgЕ антител к козьему молоку переносимость смеси «Нэнни» можно было расценивать как хорошую, что подтверждалось анамнезом — дети получали данную смесь с удовлетворительным результатом.
Выявление диагностического уровня антител к смесям на основе гидролизата белка высокой степени гидролиза, относящихся к группе лечебных смесей, отмечалось довольно редко. Однако в 6 (!) случаях все же была установлена индивидуальная непереносимость смесей из данной группы, что составляет 16,7% (!) всех наблюдений. Это подтверждает несомненный практический интерес использования данной диагностической системы. В одном случае непереносимость смеси была подтверждена клинически в процессе данного исследования и иллюстрируется клиническим примером.
Кроме того, в пределах диагностического уровня значения содержания антител к лечебным смесям также имели значительные индивидуальные различия, и представляется целесообразным учет этих данных для наиболее оптимального подбора продукта.
Алгоритм индивидуального подбора продуктов для диетотерапии детей с пищевой аллергией с учетом результатов «Лакттест» представлен на рис. 2.
Использование данного подхода позволило получить положительный результат от проводимого лечения у всех обследованных детей. За 1,5 мес наблюдения полная клиническая ремиссия была достигнута в 12 случаях, в 20 случаях отмечалась частичная ремиссия, у 4 детей можно было говорить о выраженном клиническом улучшении. Через 3 мес от начала наблюдения полная или частичная ремиссия была достигнута у всех детей. Реакций на назначаемые специализированные продукты-заменители грудного молока не отмечалось.
Проведенное исследование показало, что применение нового диагностикума — набора реагентов «Ифа-Лакттест» при обследовании детей раннего возраста с пищевой аллергией позволяет повысить эффективность аллергологического обследования, диагностировать in vitro индивидуальную переносимость конкретных продуктов детского питания и на основе этого в каждом отдельном случае индивидуально решить вопрос о возможности назначения того или иного продукта на всех этапах диетотерапии; избежать эмпирического подбора продукта из определенной группы, то есть нежелательной для ребенка смены продуктов в случае их индивидуальной непереносимости. Применение данного теста может облегчить назначение лечебного питания, например, при встречающихся в клинической практике случаях упорного отказа ребенка употреблять продукты на основе высокогидролизованного молочного белка вследствие горького вкуса. При резко негативном отношении матери к продуктам данной группы может быть подобран продукт из другой группы с учетом индивидуальной переносимости. Кроме того, тест представляет возможность врачу дать максимально точные рекомендации по подбору гипоаллергенной смеси детям с атопическим дерматитом, находящимся на грудном вскармливании в случае необходимости назначения докорма.
Использование всех вышеизложенных принципов позволяет максимально индивидуализировать побор специализированного продукта для диетотерапии детей первого года с пищевой аллергией.
По вопросам литературы обращайтесь в редакцию.
С. Г. Макарова, кандидат медицинских наук
Т. Э. Боровик, доктор медицинских наук, профессор
С. Н. Шихов, кандидат медицинских наук
Л. В. Шумилина
И. М. Гусева
А. П. Чеканникова
НЦЗД РАМН, Москва,
Медицинский научно-исследовательский центр «Медиан», Электросталь
- на какую смесь нет аллергии у грудничка
- на какую смесь перейти после грудного вскармливания в 1 месяц